Grupu modelis un piemēri
The joslas teorija ir tāda, kas nosaka cietā materiāla struktūru kopumā. To var pielietot jebkura veida cietajiem materiāliem, bet tas ir metālos, kuros tiek atspoguļoti vislielākie panākumi. Saskaņā ar šo teoriju metāliskā saite izriet no elektrostatiskās piesaistes starp pozitīvi uzlādētiem joniem un mobilajiem elektroniem kristālā..
Tāpēc metāliskam kristālam ir "elektronu jūra", kas var izskaidrot tās fiziskās īpašības. Apakšējais attēls parāda metāla saiti. Elektronu violetie punkti tiek pārvietoti jūrā, kas aptver pozitīvi uzlādētos metāla atomus.

"Elektronu jūra" veidojas no katra metāla atoma individuālajām iemaksām. Šīs iemaksas ir tās atomu orbītas. Metāla konstrukcijas parasti ir kompaktas; jo kompaktāki tie ir, jo lielāki ir to atomu mijiedarbība.
Rezultātā to atomu orbitāli pārklājas, veidojot ļoti šauras molekulārās orbītas enerģijā. Tad elektronu jūra ir tikai liels molekulāro orbītu kopums ar dažādiem enerģijas diapazoniem. Šo enerģiju diapazons veido to, ko sauc par enerģijas joslām.
Šīs joslas atrodas jebkurā kristāla reģionā, tāpēc tas tiek uzskatīts par veselumu, un no turienes nāk šīs teorijas definīcija..
Indekss
- 1 Enerģijas joslu modelis
- 1.1. Fermi līmenis
- 2 Pusvadītāji
- 2.1. Iekšējie un ārējie pusvadītāji
- 3 Piemērotās joslas teorijas piemēri
- 4 Atsauces
Enerģijas joslu modelis

Ja metāla atoma orbitālis mijiedarbojas ar tās kaimiņu (N = 2), veido divas molekulārās orbītas: viena no saitēm (zaļā josla) un viena no anti-saites (tumši sarkana josla).
Ja N = 3, tagad veidojas trīs molekulārās orbītas, no kurām vidējā (melnā josla) nav saistoša. Ja N = 4, tiek veidotas četras orbītas un tās, kurām ir vislielākais saistošais raksturs, un viena ar vislielāko sasalšanas raksturu..
Molekulārajām orbitālēm pieejamā enerģijas diapazons paplašinās, kad kristāla metāla atomi nodrošina to orbītu. Tas arī samazina enerģijas telpu starp orbitālēm līdz tādam līmenim, ka tie kondensējas joslā.
Šai joslai, kas sastāv no orbitālēm, ir zems enerģijas līmenis (zaļās un dzeltenās krāsas) un augsta enerģija (oranžās un sarkanās krāsas). Viņu enerģētiskās galējības ir mazas; tomēr lielākā daļa molekulāro orbītu (baltā josla) koncentrējas centrā.
Tas nozīmē, ka elektroni "darbojas ātrāk" caur joslas centru nekā to galos.
Fermi līmenis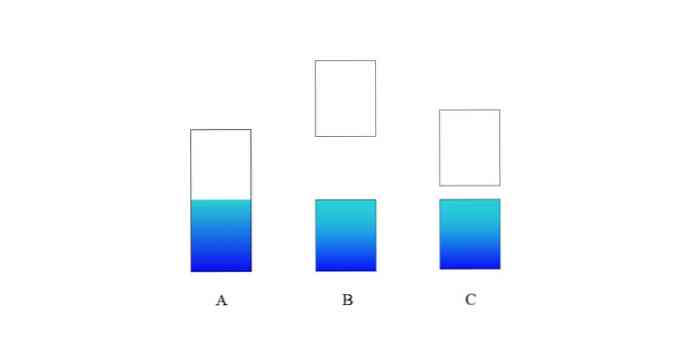
Tas ir augstākais enerģijas stāvoklis, ko aizņem elektroni cietā stāvoklī absolūtā nulles temperatūrā (T = 0 K).
Kad grupa ir būvēta, elektroni sāk aizņemt visas savas molekulārās orbītas. Ja metālam ir viens valences elektrons (-i)1) visi tās kristāla elektroni aizņems pusi no joslas.
Otra neaizņemta puse ir pazīstama kā braukšanas josla, bet elektronu pilna grupa tiek saukta par valences joslu.
Augšējā attēlā A ir tipisks valences diapazons (zils) un vadīšanas josla (balta) metāla. Zilā robežlīnija norāda Fermi līmeni.
Tā kā metāliem ir arī p-orbitāli, tie vienādi apvienojas ar p-joslu (balts).
Metālu gadījumā s un p joslas ir ļoti tuvu enerģijai. Tas ļauj to pārklāšanos, veicinot elektronus no valences joslas līdz vadīšanas joslai. Tas notiek pat temperatūrā, kas nedaudz pārsniedz 0 K.
Pārejas metāliem un no 4. \ T.
Fermi līmenis attiecībā uz vadāmības joslu ir ļoti svarīgs, lai noteiktu elektriskās īpašības.
Piemēram, metālam Z ar Fermi līmeni, kas ir ļoti tuvu vadīšanas joslai (tuvākajai tukšajai joslai enerģijā) ir augstāka elektriskā vadītspēja nekā X metālam, kurā tā Fermi līmenis ir tālu no šīs joslas..
Pusvadītāji
Tad elektriskā vadītspēja sastāv no elektronu migrācijas no valences joslas līdz vadīšanas joslai.
Ja enerģijas starpība starp abām joslām ir ļoti liela, mums ir izolācijas cietviela (tāpat kā B). No otras puses, ja šī plaisa ir salīdzinoši neliela, cietā viela ir pusvadītājs (C gadījumā)..
Saskaroties ar temperatūras pieaugumu, valences joslā esošie elektroni iegūst pietiekami daudz enerģijas, lai migrētu uz vadīšanas joslu. Tas rada elektrisko strāvu.
Faktiski tas ir cietvielu vai pusvadītāju materiālu kvalitāte: istabas temperatūrā tie ir izolatori, bet augstā temperatūrā tie ir vadītāji..
Iekšējie un ārējie pusvadītāji

Iekšējie vadītāji ir tie, kuros enerģijas starpība starp valences joslu un vadīšanas joslu ir pietiekami maza, lai siltumenerģija ļautu iziet elektronus..
No otras puses, ārējiem vadītājiem ir izmaiņas elektroniskajās struktūrās pēc dopinga ar piemaisījumiem, kas palielina to elektrisko vadītspēju. Šis piemaisījums var būt cits metāla vai nemetālisks elements.
Ja piemaisījumam ir vairāk valences elektronu, tas var nodrošināt donora joslu, kas kalpo kā tilts, lai valences joslas elektroni šķērsotu vadīšanas joslā. Šīs cietās vielas ir n veida pusvadītāji. Šeit n apzīmējums nāk no "negatīva".
Augšējā attēlā donora josla ir attēlota zilajā blokā tieši zem braukšanas joslas (tips n).
No otras puses, ja piemaisījumam ir mazāk valences elektronu, tas nodrošina akceptoru joslu, kas saīsina enerģijas starpību starp valences joslu un braukšanas joslu..
Elektroni vispirms migrē uz šo joslu, atstājot aiz "pozitīviem caurumiem", kas virzās pretējā virzienā.
Tā kā šie pozitīvie trūkumi iezīmē elektronu pāreju, cietais vai materiāls ir p-veida pusvadītājs..
Piemērotās joslas teorijas piemēri
- Paskaidrojiet, kāpēc metāli ir spilgti: to mobilie elektroni var absorbēt starojumu dažādos viļņu garumos, kad tie pāriet uz augstāku enerģijas līmeni. Tad viņi izstaro gaismu, atgriežoties zemākajos braukšanas joslas līmeņos.
- Kristāliskais silīcijs ir vissvarīgākais pusvadītāju materiāls. Ja silīcija daļu dopē ar 13. grupas elementa pēdām (B, Al, Ga, In, Tl), tas kļūst par p-veida pusvadītāju. Tā kā, ja tas ir pielīmēts ar 15. grupas elementu (N, P, As, Sb, Bi), tas kļūst par n-veida pusvadītāju.
- Gaismas diode (LED) ir kopīgs pusvadītājs p-n. Ko tu domā? Materiālam ir abu veidu pusvadītāji, gan n, gan p. Elektroni migrē no n veida pusvadītāja vadīšanas joslas līdz p veida pusvadītāja valenču joslai.
Atsauces
- Whitten, Davis, Peck & Stanley. Ķīmija (8. izdevums). CENGAGE Learning, 486-490. Lpp.
- Shiver & Atkins. (2008). Neorganiskā ķīmija (Ceturtais izdevums., Pp. 103-107, 633-635). Mc Graw kalns.
- Kuģis C. R. (2016). Cieto vielu joslas teorija. Saturs iegūts 2018. gada 28. aprīlī no: hyperphysics.phy-astr.gsu.edu
- Steve Kornic (2011). No ķīmiskajiem punktiem no ķimikāliju viedokļa. Saturs iegūts 2018. gada 28. aprīlī no: chembio.uoguelph.ca
- Vikipēdija. (2018). Ārējā pusvadītāja. Saturs iegūts 2018. gada 28. aprīlī no: en.wikipedia.org
- BYJU. (2018). Metālu joslu teorija. Saturs iegūts 2018. gada 28. aprīlī no: byjus.com



