Sudraba sulfīda (Ag2S) struktūra, īpašības, nomenklatūra, izmantošana
The sudraba sulfīds ir neorganisks savienojums, kura ķīmiskā formula ir Ag2S. Tas sastāv no melngani pelēka cieta viela, ko veido Ag katjoni+ un anjoni S2- attiecību 2: 1. S2- tas ir ļoti līdzīgs Ag+, jo abi ir mīkstie joni un tie spēj stabilizēties viens ar otru.
Sudraba rotājumi mēdz kļūt tumšāki, zaudējot raksturīgo spīdumu. Krāsu maiņa nav sudraba oksidācijas rezultāts, bet tā reakcija ar ūdeņraža sulfīdu, kas atrodas vidē zemās koncentrācijās; Tas var rasties no augiem, dzīvniekiem vai daudziem sēra saturošiem pārtikas produktiem.

H2S, kura molekulā ir sēra atoms, reaģē ar sudrabu saskaņā ar šādu ķīmisko vienādojumu: 2Ag (s) + H2S (g) => Ag2S (s) + H2(g)
Tāpēc, Ag2S ir atbildīgs par melnajiem slāņiem, kas veidojas uz sudraba. Tomēr dabā šo sēru var atrast arī minerālvielās, kas ir acantita un argentita. Abi minerāli atšķiras no daudziem citiem ar to melnajiem un gaišajiem kristāliem, piemēram, cietā krāsā augšējā attēlā.
Ag2S piedāvā polimorfas struktūras, pievilcīgas elektroniskās un optoelektroniskās īpašības, ir pusvadītājs un sola būt materiāls fotoelementu ierīču, piemēram, saules bateriju, attīstībai.
Indekss
- 1 Struktūra
- 2 Rekvizīti
- 2.1. Molekulmasa
- 2.2 Izskats
- 2.3 Smarža
- 2.4. Kušanas punkts
- 2.5. Šķīdība
- 2.6. Struktūra
- 2.7 Refrakcijas indekss
- 2.8. Dielektriskā konstante
- 2.9 Elektronika
- 2.10. Samazināšanas reakcija
- 3 Nomenklatūra
- 3.1. Sistemātika
- 3.2. Krājumi
- 3.3 Tradicionālais
- 4 Lietojumi
- 5 Atsauces
Struktūra
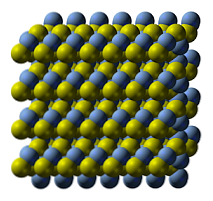
Sudraba sulfīda kristāliskā struktūra ir attēlota augšējā attēlā. Zilās sfēras atbilst Ag katjoniem+, bet dzeltenie - anjoniem S2-. Ag2S ir polimorfs, kas nozīmē, ka tā var pieņemt vairākas kristāliskas sistēmas noteiktos temperatūras apstākļos.
Kā? Ar fāzes pāreju. Joni tiek pārkārtoti tā, ka temperatūras pieaugums un cietā materiāla vibrācija netraucē elektrostatiskās piesaistes-atbaidīšanas līdzsvaru. Kad tas notiek, ir teikts, ka pastāv fāzes pāreja, un līdz ar to cietajam materiālam piemīt jaunas fizikālās īpašības (piemēram, spīdums un krāsa)..
Ag2S normālā temperatūrā (zem 179ºC) ir monokliniska kristāliska struktūra (α- Ag2S). Bez šīs cietās fāzes ir vēl divi citi: bcc (kubiskais centrs organismā) starp 179 līdz 586 ° C un fcc (kubikmetrs uz sejām) ļoti augstās temperatūrās (δ- Ag2S).
Argentīta minerāls sastāv no fcc fāzes, kas pazīstams arī kā β-Ag2S. Pēc atdzesēšanas un pārvēršanas klintī dominē to strukturālās īpašības. Tāpēc abas kristāla struktūras ir vienlaicīgas: monoklinika un bcc. Līdz ar to parādās melnās cietās daļiņas ar spilgtiem un interesantiem virsrakstiem.
Rekvizīti
Molekulmasa
247,80 g / mol
Izskats
Pelēki melni kristāli
Smarža
Tualete.
Kušanas punkts
836ºC. Šī vērtība atbilst tam, ka Ag2S ir savienojums ar nelielu jonu raksturu un līdz ar to kūst temperatūrā, kas zemāka par 1000ºC.
Šķīdība
Ūdens tikai 6.21 ∙ 10-15 g / L pie 25ºC. Tas nozīmē, ka melnās cietās vielas daudzums, kas tiek izšķīdināts, ir niecīgs. Tas atkal ir saistīts ar Ag-S saiknes mazo polāro raksturu, kur nav būtiskas atšķirības elektronegativitātē starp abiem atomiem..
Arī Ag2S nešķīst visos šķīdinātājos. Neviena molekula nevar efektīvi atdalīt kristāliskos slāņus Ag jonos+ un S2- solvāts.
Struktūra
Struktūras attēlā var redzēt arī četrus S-Ag-S obligāciju slāņus, kas pārvietojas viens ar otru, kad cietā viela ir saprotama. Šī uzvedība nozīmē, ka, neskatoties uz to, ka tā ir pusvadītājs, tā ir plastiska, tāpat kā daudzi metāli istabas temperatūrā.
S-Ag-S slāņi ir piemēroti to leņķa ģeometriju dēļ, kas tiek novērotas kā zigzags. Tiem ir sapratnes spēks, kas pārvietojas uz pārvietošanās asi, tādējādi radot jaunas, nekovalentas mijiedarbības starp sudraba un sēra atomiem.
Refrakcijas indekss
2.2
Dielektriskā konstante
6
Elektronika
Ag2S ir amfoterisks pusvadītājs, tas ir, tas darbojas tā, it kā tas būtu n un tipa p. Tas nav arī trausls, tāpēc tas ir pētīts tā pielietošanai elektroniskajās ierīcēs.
Samazināšanas reakcija
Ag2S var samazināt ar metālisku sudrabu, peldot melnās daļas ar karstu ūdeni, NaOH, alumīniju un sāli. Notiek šāda reakcija:
3Ag2S (s) + 2Al (s) + 3H2O (l) => 6Ag (s) + 3H2S (ac) + Al2O3(-i)
Nomenklatūra
Sudrabs, kura elektroniskā konfigurācija ir [Kr] 4d105s1, tā var zaudēt tikai vienu elektronu - tā attālāko orbitālu 5s. Tādējādi Ag+ paliek ar elektronisku konfigurāciju [Kr] 4d10. Tāpēc tam ir unikāls +1 valence, kas nosaka, kā tās savienojumi ir jāsauc.
Savukārt sērai ir elektroniska konfigurācija [Ne] 3s23p4, un tam ir nepieciešami divi elektroni, lai pabeigtu valences oktetu. Kad tas iegūst šos divus elektronus (no sudraba), tas pārvēršas sēra anjonā, S2-, ar konfigurāciju [Ar]. Tas ir, tas ir izoelektronisks ar argona cēlgāzi.
Tā, ka Ag2S jāsauc saskaņā ar šādām nomenklatūrām:
Sistemātika
Mērkaķissēru disudrabs Šeit mēs ņemam vērā katra elementa atomu skaitu un tiek apzīmēti ar grieķu skaitītāju prefiksu.
Krājumi
Sudraba sulfīds. Ja ir unikāla +1 valence, tā nav norādīta ar romiešu cipariem iekavās: sudraba sulfīds (I); kas ir nepareizi.
Tradicionāli
Sulfuro argéntico. Tā kā sudrabs "strādā" ar +1 valensiju, sufikss -ico tiek pievienots tā nosaukumam argentum latīņu valodā.
Lietojumi
Daži no jaunajiem Ag izmantošanas veidiem2S ir šādas:
-To nanodaļiņu (ar dažādiem izmēriem) risinājumu krāsas, ir antibakteriāla iedarbība, nav toksiskas un tādēļ tās var izmantot medicīnas un bioloģijas jomā..
-Viņu nanodaļiņas var veidot kvantu punktus. Tie absorbē un izstaro starojumu ar lielāku intensitāti nekā daudzas organiskas fluorescējošas molekulas, tāpēc tās var aizstāt tās kā bioloģiskos marķierus.
-Α-Ag struktūras2S padara to par redzamām elektroniskām īpašībām, kas izmantojamas kā saules baterijas. Tas ir arī sākumpunkts jaunu termoelektrisko materiālu un sensoru sintēzei.
Atsauces
- Mark Peplow. (2018. gada 17. aprīlis). Pusvadītāju sudraba sulfīds stiepjas kā metāls. Uzņemts no: cen.acs.org
- Sadarbība: III / 17E-17F-41C () Sudraba sulfīda (Ag2S) kristāla struktūras autori un redaktori. In: Madelung O., Rössler U., Schulz M. (eds) Non-Tetrahedrally Bonded Elements un Binary Compounds I. Landolt-Börnstein - III grupa kondensēta viela (skaitliskie dati un funkcionālās attiecības zinātnē un tehnoloģijā), vol 41C. Springer, Berlīne, Heidelberga.
- Vikipēdija. (2018). Sudraba sulfīds. Uzņemts no: en.wikipedia.org
- Stanislav I. Sadovnikov & col. (2016. gada jūlijs). Ag2S sudraba sulfīda nanodaļiņas un koloidālie šķīdumi: Sintēze un īpašības. Uzņemts no: sciencedirect.com
- Azo materiāli. (2018). Sudraba sulfīds (Ag2S) Pusvadītāji. Ņemts no: azom.com
- A. Nwofe. (2015). Sudraba sulfīdu plāno plēvju perspektīvas un izaicinājumi: pārskats. Materiālzinātnes un atjaunojamās enerģijas nodaļa, Rūpniecības fizikas katedra, Ebonyi Valsts universitāte, Abakaliki, Nigērija.
- UMassAmherst. (2011). Lekciju demonstrējumi: tīrīšana sudrabota. Uzņemts no: lecturedemos.chem.umass.edu
- Pētījums. (2018). Kas ir sudraba sulfīds? - Ķīmiskā formula un lietošanas veidi. No: study.com


