Nātrija hidrīda (NaH) īpašības, reaktivitāte, bīstamība un pielietojums
The nātrija hidrīds ir neorganisks savienojums ar formulu NaH. Tam ir jonu saite starp nātriju un hidrīdu. Tā struktūra ir attēlota 1. attēlā. Tā ir sālsūdens hidrīdu reprezentatīva, kas nozīmē, ka tas ir līdzīgs sāls saturošam hidrīdam, kas sastāv no Na + un H-joniem, atšķirībā no vairākiem molekulāriem hidrīdiem, tādiem kā borāns, metāns, amonjaks un ūdeni.
Kristāla struktūrai ir koordinācijas numurs 6, kur katru nātrija molekulu ieskauj 8 hidrīda joni ar astoņstūra formu un ir parādīti 2. attēlā (Mark Winter [Sheffield Universitāte un WebElements Ltd, 1993-2016].
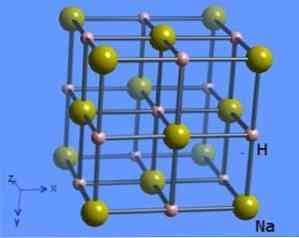
Šo savienojumu sagatavo, tieši reaģējot starp nātrija un ūdeņraža gāzi (nātrija hidrīda formula - nātrija hidrīda lietojumi, īpašības, struktūra un formula, 2005-2017):
H2 + 2Na → 2NaH
Nātrija hidrīdu pārdod komerciāli kā 60% w / w dispersijas formu (svara procentuālais svars) minerāleļļā drošai lietošanai (SODIUM HYDRIDE, s.f.).
Indekss
- 1 Nātrija hidrīda fizikālās un ķīmiskās īpašības
- 2 Reaktivitāte un bīstamība
- 3 Lietojumi
- 4 Atsauces
Nātrija hidrīda fizikālās un ķīmiskās īpašības
Nātrija hidrīds ir balts ciets, ja tas ir tīrs, lai gan parasti to iegūst pelēkā vai sudraba krāsā. Tās izskats parādīts 3. attēlā.

NaH molekulmasa ir 23,99771 g / mol, blīvums 1,396 g / ml un kušanas punkts 800 ° C (Royal Society of Chemistry, 2015). Tas nešķīst amonjaks, benzols, tetraklorīda un oglekļa disulfīds (Nacionālais biotehnoloģijas informācijas centrs, s.f.).
Savienojums ir ļoti nestabils. Tīrs NaH var viegli aizdegties gaisā. Kad tas nonāk saskarē ar gaisā esošo ūdeni, tas izdala viegli uzliesmojošu ūdeņradi.
Atverot gaisu un mitrumu, NaH ir viegli hidrolizējams arī par spēcīgu kodīgu nātrija hidroksīda (NaOH) bāzi atbilstoši reakcijai:
NaH + H2O → NaOH + H2
Šajā reakcijā var novērot, ka nātrija hidrīds darbojas kā bāze. Tas ir saistīts ar elektronegativitāti.
Nātrijam ir ievērojami zemāka elektronegativitāte (.01.0) nekā ūdeņradis (.12,1), kas nozīmē, ka ūdeņradis izdalās no elektrona blīvuma pret sevi, virzoties prom no nātrija, lai radītu nātrija katjonu un anjonu hidrīda.
Lai savienojums būtu Brønsted skābe, tai ir jānošķir elektronu blīvums no ūdeņraža, tas ir, savienot to ar elektronegatīvu atomu, piemēram, skābekli, fluoru, slāpekli utt. Tikai tad to var oficiāli aprakstīt kā H +, un vai to var atdalīt kā tādu.
Hidrīds ir daudz labāk aprakstīts kā H un tam ir bezmaksas elektronu pāris. Tā ir Brønsted bāze, nevis skābe. Faktiski, ja jūs paplašināsiet Brønsted skābes / bāzes definīciju tādā veidā, kā to darīja Lewis, jūs nonāksiet pie secinājuma, ka nātrija (Na +) ir skābes suga.
H-bāzes un H + skābes Brønsted skābes / bāzes reakcijas produkts kļūst par H2. Tā kā skābes ūdeņradis tiek ekstrahēts tieši no ūdens, ūdeņraža gāze var burbulēties, līdzsvarojot līdzsvaru pat tad, ja reakcija nav termodinamiski labvēlīga.
Var atstāt OH-jonus, kurus var rakstīt ar pārējo Na + katjonu, lai iegūtu nātrija hidroksīdu (Kāpēc reaģē ar ūdeni pamatojas uz cietā nātrija hidrīda bāzes, nevis 2016. gadā),.
Reaktivitāte un apdraudējumi
Savienojums ir spēcīgs reducētājs. Uzbrūk SiO2 stiklam. Tas aizdegas, saskaroties ar gāzveida F2, Cl2, Br2 un I2 (pēdējā temperatūrā virs 100 ° C), jo īpaši mitruma klātbūtnē, veidojot HF, HCl, HBr un HI..
Reaģē ar sēru, lai iegūtu Na2S un H2S. Tas var eksplozīvi reaģēt ar dimetilsulfīdu. Aktīvi reaģē ar acetilēnu, pat -60 ° C temperatūrā. Tas ir spontāni uzliesmojošs fluorā.
Tā sāk polimerizācijas reakciju etil-2,2,3-trifluorpropionātā, tā, ka esteris smalki sadalās. Dietilukcināta un etil-trifluoracetāta reakcijā ir radušies sprādzieni (SODIUM HYDRIDE, 2016).
Nātrija hidrīdu uzskata par kodīgu ādai vai acīm, jo reakcijas ar ūdeni var izraisīt kodīgas blakusprodukti..
Ja nokļūst acīs, tās jāmazgā ar lielu daudzumu ūdens, zem plakstiņiem vismaz 15 minūtes un nekavējoties jāmeklē medicīniskā palīdzība..
Ja nokļūst uz ādas, nekavējoties iztīriet un skaloto vietu skalojiet ar ūdeni. Ja kairinājums nepāriet, meklējiet medicīnisko palīdzību.
Tā ir kaitīga, ja norij ūdens, jo tā ir reakcija uz ūdeni. Neizraisīt vemšanu. Nekavējoties jāmeklē medicīniskā palīdzība un jānodod upuris medicīnas centram.
Nātrija hidrīda dispersija eļļā nav putekļi. Tomēr materiāls, kas reaģē, var izstarot smalku kodīgu miglu. Ieelpojot, izskalot muti ar ūdeni un nodot cietušajam vietu ar svaigu gaisu. Ir jāmeklē medicīniskā palīdzība (Rhom and Hass Inc., 2007).
Lietojumi
Nātrija hidrīda galvenais izmantojums ir kondensācijas un alkilēšanas reakciju veikšana, kas rodas, veidojot karbanonu (ko katalizē pamatne)..
Nātrija hidrīds eļļā atgādina nātrija un nātrija metālu alkoholātus, jo tas spēj darboties kā deprotonējošs līdzeklis acetoetiesterā, Claisen, Stobbe, Dieckmann un citās saistītās reakcijās. Tā ir ieguvusi priekšrocības salīdzinājumā ar citiem kondensācijas līdzekļiem, jo:
- Tā ir spēcīgāka bāze, kas izraisa tiešāku deprotonāciju.
- Nav nepieciešams pārsniegums.
- Izgatavotais H2 sniedz reakcijas lieluma mērījumu.
- Sekundārās reakcijas, piemēram, samazinājumi, tiek novērstas.
Aromātisko un heterociklisko amīnu, piemēram, 2-aminopiridīna un fenotiazīna, alkilēšana ir viegli sasniedzama ar augstu ražu, izmantojot toluola-metilformamīda maisījumus. Dimetilformamīda koncentrācija ir mainīgs, ko izmanto, lai kontrolētu reakcijas ātrumu (HINCKLEY, 1957)..
Ir ierosināts izmantot nātrija hidrīdu, lai uzglabātu ūdeņradi kurināmā elementu transportlīdzekļos, un hidrīds ir ievietots plastmasas granulās, kas sasmalcinātas ūdens klātbūtnē, lai atbrīvotu ūdeņradi..
Atsauces
- HINCKLEY, M. D. (1957). Nātrija hidrīda ražošana, apstrāde un izmantošana. Advances in Chemistry, 19, 106-117.
- Mark Winter [Šefīldas Universitāte un WebElements Ltd, U. (1993-2016)]. Nātrija: nātrija hidrīds. Izgūti no WebElements: webelements.com.
- Nacionālais biotehnoloģijas informācijas centrs. (s.f.). PubChem Compound datu bāze; CID = 24758. Izgūti no PubChem: pubchem.ncbi.nlm.nih.gov.
- Rhom un Hass inc. (2007, decembris). Nātrija hidrīda 60% dispersija eļļā. Izgūti no dow.com.
- Karaliskā ķīmijas biedrība. (2015). Nātrija hidrīds. Izgūti no ChemSpider: chemspider.com.
- NĀTRIJA. (2016). Izgūti no cameochemicals: cameochemicals.noaa.gov.
- Nātrija hidrīda formula - nātrija hidrīda izmantošana, īpašības, struktūra un formula. (2005-2017). Saturs iegūts no Softschools.com: softschools.com.
- NĀTRIJA. (s.f.). Izgūti no chemicalland21: chemicalland21.com.
- Kāpēc cietā nātrija hidrīda pamatā ir skābe, reaģējot ar ūdeni? (2016. gada 20. aprīlis). Saturs iegūts no stackexchange: chemistry.stackexchange.com.


