Gramu traipu pamats, materiāli, tehnika un pielietojums
The Grama traipi ir vienkāršākā un visnoderīgākā krāsošanas tehnika diagnostikas mikrobioloģijā. Šo tehniku radīja dāņu ārsts Hanss Christian Grams 1884. gadā, kurš spēja klasificēt baktērijas pozitīvā gramā un gramnegatīvā, atbilstoši šūnu sienas sastāvam.
Šo metodi Hucker veica 1921. gadā, lai stabilizētu reaģentus un uzlabotu traipu kvalitāti, lai Grama traipu pazīst arī kā Gram-Hucker.
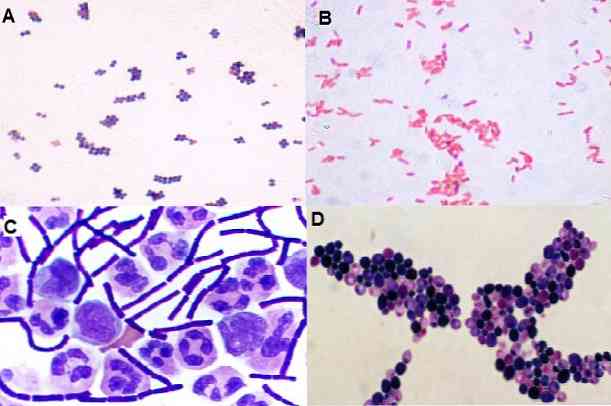
Ar šo paņēmienu ir iespējams novērot arī mikroorganismu formu, tas ir, vai tie ir koki, bacilli, kokcobacīļi, pleomorfs, pavedieni. Kā arī izplatīšana telpā: klasterī, ķēdē, izolēta, pāros, tetrados utt..
Ja ir aizdomas par bakteriālu infekciju, lielākā daļa no saņemtajiem paraugiem jāizplata uz slaida un jāpārklāj ar gramu, lai pārbaudītu mikroskopu..
Grama ziņojums palīdzēs ārstam par to, kāda veida mikroorganisms var būt infekcijas cēlonis, pirms iegūst gala rezultātu..
Dažos gadījumos pacienta dzīve ir ļoti apdraudēta, tāpēc ārstiem steidzami ir vajadzīgs Gram ziņojums, lai veiktu empīrisku ārstēšanu, gaidot mikroorganisma identifikāciju..
Piemēram, ja grams atklāj, ka cerebrospinālajā šķidrumā ir gramatiski pozitīvi koki, ārsts orientēs sākotnējo terapiju ar antibiotikām, kas novērš šāda veida baktērijas, saskaņā ar tam noteiktajiem protokoliem..
Kad gala rezultāts nonāk ar izolētā mikroorganisma nosaukumu un attiecīgo antibiotiku, ārsts novērtēs, vai mainīt terapiju. Šis lēmums tiks pieņemts saskaņā ar pētījumu par mikroorganisma jutību pret antibiotikām, ko tā saņem, un pacienta attīstību..
Indekss
- 1 Fonds
- 2 Materiāli
- 3 Krāsvielu un reaģentu sagatavošana
- 3.1. Kristāla violets šķīdums
- 3.2. Jodo-Lugols
- 3.3 Balināšana
- 3.4 Kontrasts
- 4 Reaģentu uzglabāšana
- 5 Krāsojamā parauga izplatīšanās sagatavošana
- 5.1. Tiešo paraugu grams
- 5.2. Kultūru grams
- 6 Tehnika
- 7 Lietderība
- 8 Biežas kļūdas
- 9 Atsauces
Fonds
Šī ir metode, kas piedāvā 4 fundamentālus soļus: iekrāsošanu, fiksāciju ar mordantu, krāsas maiņu un kontracepciju. Tāpēc šī metode papildus baktēriju krāsošanai atšķir arī tos.
Kristāla violets ir pirmā izmantotā krāsviela. Tam ir afinitāte pret peptidoglikānu un purpursarkanā krāsā notiks visas esošās baktērijas, tad tiek novietots bagols, kas darbojas kā sāpīgs, tas ir, tas izraisīs nešķīstošu kristāla violeta joda - ribonukleāro proteīnu kompleksu veidošanos šūnā..
Gram-pozitīvās baktērijas ar biezu peptidoglikāna sienu veido vairākus kompleksus (kristālviolet-jodu), tāpēc tie saglabā krāsu.
Tas ietekmē arī to, ka Gram-pozitīvās baktēriju sienas satur lielāku nepiesātināto skābju daudzumu, kas uzrāda augstu afinitāti pret oksidētājiem (Lugol).
Tikmēr gramnegatīvajām baktērijām ir plāns peptidoglikāna slānis, kas padara baktērijas mazāk sarežģītas nekā Gram-pozitīvās baktērijas..
Tad nāk krāsas maiņas solis, kur Gram-pozitīvās un gramnegatīvās baktērijas darbojas atšķirīgi.
Gram-negatīvās baktērijas satur ārējo membrānu, kas ir bagāta ar lipopolisaharīdiem, kas ir daļa no tās šūnu sienas. Tauki tiek iznīcināti, saskaroties ar alkohola acetonu, tāpēc ārējā membrāna ir destabilizēta, atbrīvojas violets kristāls.
Tādā veidā tas ir kontrastēts ar safranīnu vai pamata fuksīnu, ņemot sarkano krāsu.
Gram-pozitīvo baktēriju gadījumā tās iztur pret krāsas izmaiņām, jo balinātājs darbojas, lai aizvērtu poras, kas novērš kristāla violeta / joda kompleksu izplūšanu.
Tāpēc krāsa ar violetu kristālu ir stabila, un nav vietas safranīnam vai fuksīnam. Šī iemesla dēļ šīs baktērijas krāso intensīvu zilu vai violetu.
Materiāli
Grama krāsošanas komplekts sastāv no:
- Violetais kristāls
- Lugol
- Acetona spirts
- Safranīns vai pamata fuksīns
Krāsu un reaģentu sagatavošana
Kristāla violets šķīdums
A risinājums:
Violetais kristāls -2 gr
Etilspirts 95% -20cc
B risinājums:
Amonija oksalāts -0,8 gr
Destilēts ūdens - 80 cm3
Violetā kristāla gala sagatavošanai 1:10 šķīdums jāatšķaida ar destilētu ūdeni un jāsamaisa ar 4 daļām B šķīduma. Maisījumu pirms lietošanas uzglabā 24 stundas. To filtrē kolbā dzintara krāsošanai, izmantojot papīra filtru.
Dienu, kas tiks izmantots katru dienu, pārnes uz dzintara pudeli ar pilinātāju.
Jodo-Lugols
Nosver un mēra katra savienojuma norādīto daudzumu:
Iodo kristāli - 1gr
Kālija jodīds - 2gr
Destilēts ūdens -300 cm3
Kālija jodīds nedaudz izšķīst ūdenī un tad pievieno jodu. Šķīdumu noskalo ar dzintara krāsas pudeli.
Dienu, kas tiks izmantots katru dienu, pārnes uz mazāku dzintara pudeli ar pilinātāju.
Balināšana
95% etilspirta -50 ml
Acetons - 50 ml
Tas ir sagatavots vienādās daļās. Nosedziet, tā tiecas iztvaikot.
Novietojiet pudeli ar pilinātāju.
Šis preparāts nodrošina krāsas maiņu vidēji 5-10 sekunžu laikā, un tas ir visvairāk ieteicams.
Iesācēji dod priekšroku izmantot tikai 95% etilspirtu, kur krāsas izmaiņas ir lēnākas no 10 līdz 30 sekundēm.
Kaut arī pieredzējušākie var izmantot tīru acetonu, kur krāsas izmaiņas notiek ļoti ātri no 1 līdz 5 sekundēm.
Kontrasts
Safranīna izejas šķīdums
Safranina -2,5 gr
Etilspirts 95% -100 cm3
Pēc svēršanas norādītais safranīna daudzums izšķīst 100 ml etilspirta līdz 95%..
Darbīgo safranīna šķīdumu pagatavo no izejas šķīduma.
Lai to izdarītu, izmēra 10 cc izejas šķīduma, pievieno 90 ml destilēta ūdens, lai pabeigtu 100 ml.
Ieteicams katru dienu pārvietot dzintara pudeli ar pilinātāju.
Mikroorganismi, kas Gram-Hucker traipu veidā vāji vājina Gram-negatīvu, piemēram, dažus anaerobus, Legionella sp, Campylobacter sp un Brucella sp, tos var daudz labāk krāsot, ja tiek izmantota Kopeloffa veiktā modifikācija Gram-Hucker krāsošanai, ko sauc par Gram-Kopeloffu..
Šī metode maina safranīna krāsu ar pamata fuksīnu. Ar šo modifikāciju ir iespējams efektīvi krāsot iepriekšminētos mikroorganismus.
Reaģentu uzglabāšana
Sagatavotās krāsvielas jāuzglabā istabas temperatūrā.
Parauga sagatavošana izplatās uz krāsu
Paraugam jābūt vismaz 10. \ T5 mikroorganismu novērošana, pirms mikroorganismu novērošana uztriepēs ir iespējama. Izplatījumus var izgatavot no tieša parauga vai kultūru cietā vai šķidrā vidē.
Izkliedēm jābūt vienādām, labi izkliedētām un ne pārāk biezām, lai labāk attēlotu esošās struktūras.
-Tiešo paraugu grams
Urīna grams bez centrifūgas
Urīns ir sajaukts un 10 µl tiek novietots uz slaida. Vismaz vienas baktērijas / iegremdēšanas lauka novērošana norāda, ka ir infekcija.
Tas nozīmē, ka kultūrai būs aptuveni vairāk nekā 100 000 KVV / ml (10. \ T5 CFU / ml) urīnā 85% gadījumu.
Šī metode nav noderīga koloniju skaitam, kas ir mazāks par 100 000 CFU.
LCR grams
CSF jācentrifugē, supernatants jānoņem un granulas jāpārklāj uz slaida. Šis šķidrums normālos apstākļos ir sterils; baktēriju novērošana norāda uz infekciju.
Grammas elpceļu paraugi
Diagnozē vienmēr vadīs krūts gramu, bronhu vai bronhu-alveolāro skalošanu, lai gan var būt dažādi mikroorganismi, turklāt tā ir noderīga novērojamo šūnu tipam..
Krēpu gadījumā uztriepes jāsagatavo, izmantojot paraugu, kas ir visvairāk strutainas.
Stool Gram
Nav ieteicams veikt Gram uz šāda veida paraugiem, jo tam nav diagnostikas vērtības.
-Grams
Tos var izdarīt divos veidos: vienu no šķidrajām kultūrām un otru no cietajām kultūrām.
Šķidras kultūras
No šķidrajām kultūrām tā ir ļoti vienkārša; zem gaišākas kārtas tiek paņemti vairāki duļķaina buljona cepumi, un tie tiek novietoti uz tīra un sausa slaida, kas nodrošina apļveida kustības no centra uz perifēriju, lai vienmērīgi izplatītu materiālu.
Tam ir atļauts spontāni izžūt gaisā. Pēc sausuma materiāls tiek piestiprināts pie lokšņu ar siltumu. Šim nolūkam ar spailes palīdzību 3 loksne tiek nodota 4 reizes caur Bunsen degļa liesmu, rūpējoties par to, lai netiktu sadedzināts materiāls..
Lokai ļauj atdzist un novietot uz krāsošanas tilta.
Cietie kultūraugi
Lai veiktu paplašinājumu Grama krāsai no cietas kultūras, rīkojieties šādi:
Pirms izvēlēties kolonijas, kas jāizmanto, jāsagatavo slaidu, ievietojot divus pilienus aptuveni sterilā fizioloģiskā sāls šķīdumā..
Ja sākotnējā kultūras plāksnē ir vairāki dažādi koloniju veidi, tad katrai no tām tiks izvēlēta izolēta kolonija, lai veiktu gramu. Katra kolonija tiks ņemta ar platīna cilpu, lai to izšķīdinātu sāls šķīdumā, kas iepriekš novietots uz slaida.
No centra līdz perifērijai tiek dotas apļveida kustības, lai koloniju sadalītu vienādi uz slaida..
Tam ir atļauts spontāni izžūt gaisā. Pēc žāvēšanas loksne tiek fiksēta ar karstumu, kā paskaidrots iepriekš (liesmojošs slaids ar šķiltavu), uzmanoties, lai nesadedzinātu materiālu.
Šī procedūra jāveic ar katru citu kolonijas veidu. Uz papīra lapas jānorāda novērotā secība, piemēram:
1. kolonija: dzeltenā beta-hemolītiskā kolonija: Gram-pozitīvi koki tika novēroti klasteros
2. kolonija: krēmu kolonija bez hemolīzes: tika novērota gramnegatīva kokcobacīlija.
Katrai lapai jābūt marķētai, lai zinātu, ko mēs novērojam.
Tehnika
Grama krāsošanas tehnika ir ārkārtīgi vienkārša un salīdzinoši lēta, un to nevar palaist garām mikrobioloģijas laboratorijā.
To dara šādi:
- Piestipriniet uztriepes ar karstumu un novietojiet uz krāsaina tilta.
- Loksne pilnībā pārklāta ar violetu stiklu 1 minūti.
- Mazgāt ar ūdeni. Nežāvējiet
- Novietojiet plāksni ar Lugol šķīdumu, atstājiet uz 1 minūti. Mazgāt ar ūdeni. Nežāvējiet.
- 5-10 sekundes sajauciet ar vieglu maisīšanos acetona spirta veidā. Vai ievietojiet loksni vertikālā stāvoklī un nometiet pilienu no krāsas, kas samazinās, līdz atlikušais violets stikls tiek vilkts. Nepārsniedziet.
- Mazgāt ar ūdeni. Nežāvējiet.
- Nomainiet loksni uz krāsainā tilta un uz 30 sekundēm pārklājiet ar safranīnu (Gram-Hucker) vai 1 min ar pamata fuksīnu (Gram-Kopeloff).
- Mazgāt ar ūdeni
- Ļaujiet spontāni izžūt vertikālā gaisā.
Pēc žāvēšanas ievietojiet 1 pilienu iegremdēšanas eļļas, lai to ievērotu saskaņā ar mērķi 100X optiskajā mikroskopā.
Lietderība
Šī metode ļauj atšķirt lielāko daļu baktēriju morfotērijas atšķirības.
Raugi arī atšķiras ar šo krāsu. Viņi paņem kristālvioleti, tas ir, pozitīvi Gramu.
No otras puses, var izšķirt Grama pozitīvās sporas veidojošās bacīles, kurās bacillus iekšpusē ir vērojama skaidra telpa, kur veidojas endospore, lai gan sporas labi nespiež. Lai izmantotu sporas, tiek izmantotas citas metodes, piemēram, Shaeffer-Fulton.
Jāatzīmē, ka šis traipu veids nedod visu veidu baktērijas, proti, ir gadījumi, kad krāsošana nedarbojas.
Šajā gadījumā var minēt baktērijas, kurām nav šūnu sienas. Piemēram: Mycoplasma ģints, sferoplasti, ureaplasma, L-formas un protoplasti.
Tā arī krāso slikti baktērijas ar sienām, kurās ir bagātīgas mikolskābes, piemēram, mikobaktērijas un intracelulāras baktērijas, piemēram, Chlamydias un Rickettsias..
Tas ir arī neefektīvs, lai krāsotu lielāko spirochetālo baktēriju.
Ir tādas pašas ģints baktērijas, kuras var novērot tajā pašā paraugā kā Gram pozitīvs un kā Gram negatīvs. Ja tas notiek, to sauc par mainīgo Gram traipu, ko var izraisīt barības vielu izmaiņas, temperatūra, pH vai elektrolītu koncentrācija..
Bieži pieļautas kļūdas
Pārmērīgi balināt
Pārspīlēšana krāsas maiņas posmā var izraisīt viltus gramnegatīvus mikroorganismus.
Negaidiet pietiekami daudz žāvēšanas laika, lai pievienotu iegremdēšanas eļļu:
Šī kļūda izraisa tauku micellu veidošanos, kas apgrūtina esošo struktūru novērošanu. Tas notiek, kad eļļa pievienojas uztriepes esošajām ūdens molekulām.
Atgrieziet reaģentu secību:
Šāda kļūda radīs gramnegatīvas baktērijas, lai parādītu violetu, tas ir, viltus Gram-pozitīvu.
Izmantot vecās kultūras (cietas vai šķidras):
Tas var izraisīt Gram-pozitīvās baktērijas Gram negatīvas (viltus gramnegatīvas) traipus. Tas notiek tāpēc, ka vecajās kultūrās ir iespējams, ka baktērijas ir mirušas vai pasliktinājušās, un šajos apstākļos baktērijas nesaglabā violetu kristālu..
Izmantojiet ļoti vecu Lugol risinājumu:
Laika gaitā bagāža zaudē savas īpašības un tās krāsa zūd. Ja tiek izmantots jau deģenerētais reaģents, tas nenostiprina kristālvioleti labi, tāpēc ir iespēja iegūt nepatiesu mikroorganismu vizualizāciju Gram-negatīvs.
Zilā fona
Pareizi mainīts fons būs sarkans. Zils fons norāda, ka krāsas maiņa bija nepietiekama.
Atsauces
- Ryan KJ, Ray C. 2010. Sherris. Mikrobioloģija Medicīna, 6. izdevums McGraw-Hill, Ņujorka, ASV
- Koneman E, Allen S, Janda W, Schreckenberger P, Winn W. (2004). Mikrobioloģiskā diagnoze. (5. izdevums). Argentīna, Redakcijas Panamericana S.A..
- Forbes B, Sahm D, Weissfeld A. 2009. Bailey & Scott mikrobioloģiskā diagnoze. 12 ed. Argentīna Panamericana S.A Redaktors
- Casas-Rincón G. 1994. Vispārējā mikoloģija. 2. izdevums Universidad Central de Venezuela, bibliotēkas izdevumi. Venecuēla, Karakasa.
- "Gramu traipi" Vikipēdija, brīvā enciklopēdija. 4. oktobris, 2018, 23:40 UTC. 2018. gada 9. decembris, 17:11. Uzņemts no es.wikipedia.org.
- González M, González N. 2011. Medicīniskās mikrobioloģijas rokasgrāmata. 2. izdevums, Venecuēla: Karabobo Universitātes Mediju un publikāciju direkcija.
- López-Jácome L, Hernández-Durán M, Colín-Castro C, Ortega-Peña S, Cerón-González G, Franco-Cendejas F. Pamata krāsošana mikrobioloģijas laboratorijā. Invaliditātes pētījumi. 2014; 3 (1): 10-18.


