Bioloģiskā katalizatora veiktspēja un piemēri
A bioloģiskais katalizators o biokatalizators ir olbaltumvielu izcelsmes molekula, kurai ir spēja paātrināt ķīmiskās reakcijas, kas rodas dzīvo būtņu iekšienē. Katalizatora olbaltumvielu molekulas ir fermenti, un RNS raksturs ir ribozīms. Šajā rakstā mēs pievērsīsimies fermentu izpētei, kas ir vislabāk zināmi bioloģiskie katalizatori.
Ja nav fermentu, nevarētu notikt milzīgs skaits reakciju, kas notiek šūnā un kas ļauj dzīvi. Tie ir atbildīgi par procesa paātrināšanu pēc lieluma apmēram 106 - un dažos gadījumos daudz lielāks.
Indekss
- 1 Katalīze
- 2 Fermenti
- 2.1. Kas ir enzīms?
- 2.2 Enzīmu raksturojums
- 2.3 Enzīmu nomenklatūra un klasifikācija
- 2.4 Kā darbojas fermenti?
- 2.5 Enzīmu inhibitori
- 2.6 Piemēri
- 3 Bioloģisko katalizatoru (fermentu) un ķīmisko katalizatoru atšķirība
- 3.1 Reakcijas, ko katalizē fermenti, notiek ātrāk
- 3.2 Lielākā daļa fermentu darbojas fizioloģiskos apstākļos
- 3.3. Specifiskums
- 3.4 Enzīmu regulēšana ir precīza
- 4 Atsauces
Katalīze
Katalizators ir molekula, kas spēj mainīt ķīmiskās reakcijas ātrumu, neizmantojot minēto reakciju.
Ķīmiskās reakcijas ietver enerģiju: reakcijā iesaistītās sākotnējās molekulas vai reaģenti sākas ar zināmu enerģijas līmeni. Papildu enerģijas daudzums tiek absorbēts, lai sasniegtu "pārejas stāvokli". Pēc tam enerģija tiek izlaista ar produktiem.
Enerģijas starpība starp reaģentiem un produktiem tiek izteikta kā ΔG. Ja produktu enerģijas līmenis ir lielāks nekā reaģenti, reakcija ir endergoniska, nevis spontāna. Turpretī, ja produktu enerģija ir zemāka, reakcija ir eksergoniska un spontāna.
Tomēr, ja reakcija ir spontāna, tas nenozīmē, ka tas notiks ar ievērojamu ātrumu. Reakcijas ātrums ir atkarīgs no ΔG * (zvaigznīte attiecas uz aktivizēšanas enerģiju).
Lasītājam ir jāpatur prātā šie jēdzieni, lai saprastu, kā notiek fermentu darbība.
Fermenti
Kas ir enzīms?
Fermenti ir neticami sarežģītas bioloģiskas molekulas, kas sastāv galvenokārt no olbaltumvielām. Proteīni, savukārt, ir garas aminoskābju ķēdes.
Viena no izcilākajām fermentu īpašībām ir to specifika mērķa molekulā - šo molekulu sauc par substrātu.
Fermentu raksturojums
Fermenti pastāv vairākos veidos. Daži no tiem sastāv tikai no olbaltumvielām, bet citos - ne proteīniem, ko sauc par kofaktoriem (metāli, joni, organiskās molekulas utt.)..
Tādējādi apoenzīms ir enzīms bez tā kofaktora, un apoenzīma un tā kofaktora kombināciju sauc par holoenzīmu..
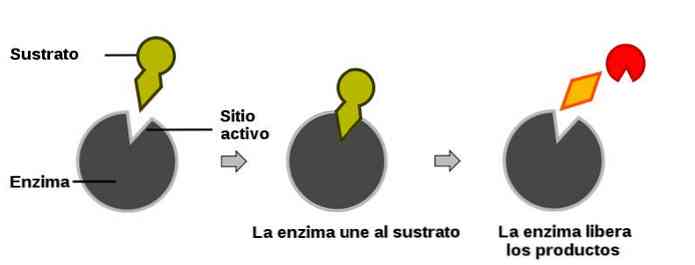
Tie ir ievērojami lielas molekulas. Tomēr tikai neliela fermenta vieta tieši piedalās reakcijā ar substrātu, un šis reģions ir aktīvā vieta.
Kad reakcija sākas, fermentu savieno ar savu substrātu, jo atslēga ir savienota ar tās bloķēšanu (šis modelis ir faktiskā bioloģiskā procesa vienkāršošana, bet kalpo, lai ilustrētu procesu).
Visas ķīmiskās reakcijas, kas rodas mūsu organismā, katalizē fermenti. Patiesībā, ja šīs molekulas nebūtu, mums būtu jāgaida simtiem vai tūkstošiem gadu, lai reakcijas būtu pabeigtas. Tāpēc fermentu aktivitātes regulēšana ir jākontrolē ļoti specifiskā veidā.
Fermentu nomenklatūra un klasifikācija
Kad mēs redzam molekulu, kuras nosaukums beidzas ar -ase, mēs varam būt pārliecināti, ka tas ir enzīms (lai gan šim noteikumam ir izņēmumi, piemēram, tripsīns). Šī ir konvencija, lai apzīmētu fermentu nosaukumu.
Pastāv seši galvenie fermentu veidi: oksidoreduktāzes, transferāzes, hidrolāzes, liāzes, izomerāzes un ligāzes; atbildīgas par: redoksreakcijām, atomu pārnesei, hidrolīzei, dubultās saites pievienošanai, molekulu izomerizācijai un saistīšanai;.
Kā darbojas fermenti?
Sadaļā par katalīzi mēs minējām, ka reakcijas ātrums ir atkarīgs no ΔG * vērtības. Jo augstāka šī vērtība, jo lēnāka un lēnāka reakcija. Enzīms ir atbildīgs par minētā parametra samazināšanu, tādējādi palielinot reakcijas ātrumu.
Atšķirība starp produktiem un reaģentiem paliek identiska (fermentu neietekmē), tāpat kā to sadale. Ferments veicina pārejas stāvokļa veidošanos.
Enzīmu inhibitori
Enzīmu izpētes kontekstā inhibitori ir vielas, kas spēj samazināt katalizatora aktivitāti. Tos iedala divos veidos: konkurētspējīgi un nekonkurējoši inhibitori. Tie, kas ir pirmie, konkurē ar substrātu, bet citi to nedara.
Parasti inhibēšanas process ir atgriezenisks, lai gan daži inhibitori gandrīz nemainīgi var būt saistīti ar fermentu.
Piemēri
Mūsu šūnās - un visu dzīvo būtņu šūnās - ir liels daudzums fermentu. Tomēr vislabāk zināmi ir tie, kas piedalās tādos metabolisma ceļos kā glikolīze, Krebsa cikls, elektronu transportēšanas ķēde, cita starpā..
Sukcināta dehidrogenāze ir oksidoredukta tipa enzīms, kas katalizē sukcināta oksidēšanos. Šajā gadījumā reakcija ietver divu ūdeņraža atomu zudumu.
Bioloģisko katalizatoru (fermentu) un ķīmisko katalizatoru atšķirība
Ir ķīmiskas dabas katalizatori, kas, tāpat kā bioloģiskie, palielina reakciju ātrumu. Tomēr pastāv ievērojamas atšķirības starp abiem molekulu veidiem.
Enzīmu katalizētas reakcijas notiek ātrāk
Pirmkārt, fermenti spēj palielināt reakciju ātrumu, kas ir aptuveni 106 līdz 1012. Ķīmiskie katalizatori arī palielina ātrumu, bet tikai dažus lielumus.
Lielākā daļa fermentu darbojas fizioloģiskos apstākļos
Tā kā bioloģiskās reakcijas tiek veiktas dzīvo būtņu iekšienē, to optimālie apstākļi aptver temperatūras un pH fizioloģiskās vērtības. No otras puses, ķīmiķiem ir vajadzīgi krasi temperatūras, spiediena un skābuma apstākļi.
Specifiskums
Fermenti ir ļoti specifiski reakcijās, ko tie katalizē. Vairumā gadījumu viņi strādā tikai ar vienu substrātu vai ar dažiem. Šī specifika attiecas arī uz to ražoto produktu veidu. Ķīmisko katalizatoru substrātu klāsts ir daudz plašāks.
Spēki, kas nosaka mijiedarbības specifiku starp fermentu un tā substrātu, ir tādi paši, kas nosaka tā paša proteīna konformāciju (Van der Waals mijiedarbība, elektrostatiskās, ūdeņraža saites un hidrofobie).
Enzīmu regulēšana ir precīza
Visbeidzot, fermentiem ir lielāka regulēšanas spēja un to aktivitāte atšķiras atkarībā no dažādu vielu koncentrācijas šūnā.
Regulējošo mehānismu vidū mēs atrodam allosterisko kontroli, fermentu kovalento modifikāciju un sintezētā fermenta daudzuma izmaiņas..
Atsauces
- Berg, J. M., Stryer, L., un Tymoczko, J. L. (2007). Bioķīmija. Es mainīju.
- Campbell, M. K., & Farrell, S. O. (2011). Bioķīmija Sestais izdevums. Thomson. Brooks / Cole.
- Devlin, T. M. (2011). Bioķīmijas mācību grāmata. John Wiley & Sons.
- Koolman, J., & Röhm, K. H. (2005). Bioķīmija: teksts un atlants. Ed. Panamericana Medical.
- Mougios, V. (2006). Vingrojumu bioķīmija. Cilvēka kinētika.
- Müller-Esterl, W. (2008). Bioķīmija Medicīnas un dzīvības zinātņu pamati. Es mainīju.
- Poortmans, J.R. (2004). Vingrošanas bioķīmijas principi. Karger.
- Voet, D., & Voet, J. G. (2006). Bioķīmija. Ed. Panamericana Medical.


