Slāpekļa oksīdi (NOx) Dažādi preparāti un nomenklatūras
The slāpekļa oksīdi tie būtībā ir gāzveida neorganiskie savienojumi, kas satur saites starp slāpekļa un skābekļa atomiem. Tās ķīmiskā formula ir NOx, norādot, ka oksīdiem ir atšķirīga skābekļa un slāpekļa proporcija.
Slāpeklis vada periodiskās tabulas 15. grupu, bet skābekļa grupa 16; abi elementi ir 2. perioda dalībnieki. Šis tuvums ir iemesls, kāpēc N-O saites oksīdos ir kovalenti. Tādā veidā slāpekļa oksīdu saites ir kovalenti.
Visas šīs saiknes var izskaidrot, izmantojot molekulārās orbitālās teorijas, kas atklāj paramagnetismu (elektronu, kas pēdējo molekulāro orbitāli nav savienots) dažiem no šiem savienojumiem. No tiem visbiežāk sastopamie savienojumi ir slāpekļa oksīds un slāpekļa dioksīds.
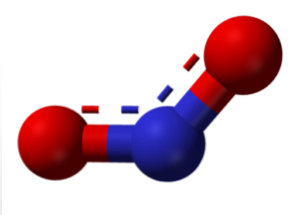
Augšējā attēlā esošā molekula atbilst leņķiskajai struktūrai slāpekļa dioksīda gāzes fāzē (NO2). Turpretim slāpekļa oksīdam (NO) ir lineāra struktūra (ņemot vērā spibridizāciju abiem atomiem)..
Slāpekļa oksīdi ir daudzas cilvēka darbības rezultātā radītas gāzes, sākot no transportlīdzekļa vadīšanas vai cigarešu smēķēšanas, līdz rūpnieciskiem procesiem kā piesārņojošiem atkritumiem. Tomēr NO dabiski rada fermentu reakcijas un zibens pērkona negaiss: N2(g) + O2(g) => 2NO (g)
Augstās staru temperatūras izjauc enerģētisko barjeru, kas novērš šīs reakcijas rašanos normālos apstākļos. Kāda enerģijas barjera? To veido trīskāršā saite N≡N, veidojot N-molekulu2 inertas gāzes no atmosfēras.
Indekss
- 1 Oksidācijas skaitļi slāpekļa un skābekļa oksīdiem
- 2 Dažādi formulējumi un nomenklatūras
- 2.1 Slāpekļa oksīds (N2O)
- 2.2 Slāpekļa oksīds (NO)
- 2.3 Slāpekļa trioksīds (N2O3)
- 2.4. Dioksīds un slāpekļa tetoksīds (NO2, N2O4)
- 2.5. Slāpekļa pentoksīds (N2O5)
- 3 Atsauces
Slāpekļa un skābekļa oksidācijas numuri to oksīdos
Skābekļa elektroniskā konfigurācija ir [2]22p4, kam nepieciešams tikai divi elektroni, lai pabeigtu tās valences čaulas oktetu; tas ir, tas var iegūt divus elektronus un oksidācijas numurs ir vienāds ar -2.
No otras puses, slāpekļa elektroniskā konfigurācija ir [2]22p3, spēja iegūt līdz trim elektroniem, lai aizpildītu savu valences oktetu; piemēram, amonjaka gadījumā (NH3) oksidācijas numurs ir vienāds ar -3. Bet skābeklis ir daudz elektronegatīvāks nekā ūdeņradis un "piespiež" slāpekli dalīties ar saviem elektroniem.
Cik daudz elektronu var slāpēt ar skābekli? Ja koplietojat savas valences apvalka elektronus pa vienam, sasniegsiet piecu elektronu robežu, kas atbilst +5 oksidācijas skaitam..
Līdz ar to, atkarībā no tā, cik daudz savienojumu veidojas ar skābekli, slāpekļa oksidācijas skaitļi svārstās no +1 līdz +5.
Dažādi formulējumi un nomenklatūras
Slāpekļa oksīdi, palielinoties slāpekļa oksidācijas skaitam, ir šādi:
- N2Vai arī slāpekļa oksīds (+1)
- NĒ, slāpekļa oksīds (+2)
- N2O3, dinitrīna trioksīds (+3)
- NĒ2, slāpekļa dioksīds (+4)
- N2O5, dentogēna pentoksīds (+5)
Slāpekļa oksīds (N. \ T2O)
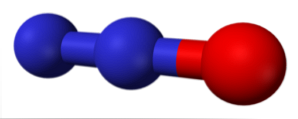
Slāpekļa oksīds (vai pazīstams kā smejas gāze) ir bezkrāsains gāze ar nelielu saldu smaržu un maz reaktīvu. To var vizualizēt kā N molekulu2 (zilas sfēras), kas vienā galā ir pievienojis skābekļa atomu. To sagatavo, izmantojot termiskā nitrātu sāļu sadalīšanos, un to izmanto kā anestēzijas līdzekli un pretsāpju līdzekli.
Slāpeklim šajā oksīdā ir oksidācijas skaits +1, kas nozīmē, ka tas nav ļoti oksidēts, un tā pieprasījums pēc elektroniem nav pārliecinošs; tomēr, lai kļūtu par stabilu molekulāro slāpekli, jums ir jāiegūst tikai divi elektroni (viens katram slāpeklim).
Bāzes un skābes šķīdumos reakcijas ir:
N2O (g) + 2H+(ac) + 2e- => N2(g) + H2O (l)
N2O (g) + H2O (l) + 2e- => N2(g) + 2OH-(ac)
Šīs reakcijas, kaut arī termodinamiski, veicina stabilas molekulas N veidošanās2, reaģenti, kas nodod elektronu pāri, ir ļoti spēcīgi reducētāji.
Slāpekļa oksīds (NO)
Šis oksīds sastāv no bezkrāsainas, reaktīvas un paramagnetiskas gāzes. Tāpat kā slāpekļa oksīdam, tam ir lineāra molekulārā struktūra, bet ar lielu atšķirību, ka N = O saitei ir arī trīskāršā saite..
NO ātri oksidējas gaisā, lai iegūtu NO2, un tādējādi radītu stabilākas molekulāras orbītas ar vairāk oksidētu slāpekļa atomu (+4).
2NO (g) + O2(g) => 2NO2(g)
Biochemiskie un fizioloģiskie pētījumi ir pamatā šī oksīda labvēlīgajai lomai dzīvajos organismos.
Tā nespēj veidot N-N saites ar citu NO molekulu, jo nesalīdzinātais elektrons tiek pārvietots molekulārajā orbitālajā virzienā, kas vairāk vērsts uz skābekļa atomu (tā augstās elektronegativitātes dēļ). Pretēji notiek NO2, kas var veidot gāzveida dimērus.
Slāpekļa trioksīds (N. \ T2O3)
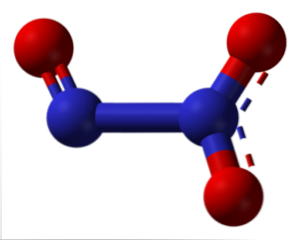
Struktūras punktveida līnijas norāda uz divkāršās saites rezonansi. Tāpat kā visiem atomiem, tiem ir spibridizācija2, molekula ir plakana un molekulārā mijiedarbība ir pietiekami efektīva, lai slāpekļa trioksīds būtu zilā krāsā zem -101ºC. Augstākās temperatūrās tā kūst un disociējas NO un NO2.
Kāpēc tas ir sadalīts? Tā kā oksidācijas skaitļi +2 un +4 ir stabilāki nekā +3, pēdējais ir oksīdā katram no diviem slāpekļa atomiem. To atkal var izskaidrot ar disproporcijas izraisīto molekulāro orbītu stabilitāti.
Attēlā N kreisā puse2O3 atbilst NO, bet labajā pusē - NO2. Loģiski, ka to iegūst, apvienojot iepriekšējos oksīdus ļoti aukstā temperatūrā (-20ºC). N2O3 ir slāpekļskābes anhidrīds (HNO)2).
Dioksīds un slāpekļa tetoksīds (NO. \ T2, N2O4)
NĒ2 tā ir brūna vai brūna gāze, reaktīva un paramagnetiska. Tā kā tam ir nesavienots elektrons, tas dimerizējas (saistās) ar citu NO gāzveida molekulu2 veidot bezkrāsainu gāzi slāpekļa tetoksīdu, nosakot līdzsvaru starp abām ķīmiskām sugām: \ t
2NO2(g) <=> N2O4(g)
Tas ir indīgs un daudzpusīgs oksidētājs, kas spēj disproporcionēt redoksreakcijas jonos (oksoānos).2- un NO3- (radot skābo lietus), vai NO.
Tāpat NO2 ir iesaistīta sarežģītās atmosfēras reakcijās, kas izraisa ozona koncentrācijas izmaiņas (OR3) pie sauszemes un stratosfērā.
Ditrogēnpentoksīds (N. \ T2O5)
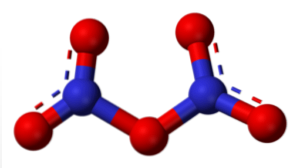
Hidratējot tas rada HNO3, un augstākā skābes koncentrācijā skābeklis galvenokārt protonējas ar daļēju pozitīvu lādiņu -O+-H, paātrinot redoksreakcijas
Atsauces
- AskIITians. ((2006-2018)). AskIITians. Ielādēts 2018. gada 29. martā no askIITians: askiitians.com
- Encyclopaedia Britannica, Inc. (2018). Encyclopaedia Britannica. Saturs iegūts 2018. gada 29. martā no Encyclopaedia Britannica: britannica.com
- Tox Town. (2017). Tox Town. Ielādēts 2018. gada 29. martā no Tox Town: toxtown.nlm.nih.gov
- Profesors Patricia Shapley. (2010). Slāpekļa oksīdi atmosfērā. Ilinoisas Universitāte. Saturs iegūts 2018. gada 29. martā no: butane.chem.uiuc.edu
- Shiver & Atkins. (2008). Neorganiskā ķīmija In 15. grupas elementi. (Ceturtais izdevums., 361. - 366. lpp.). Mc Graw kalns