Kalcija oksīda (CaO) struktūra, īpašības un lietošanas veidi
The kalcija oksīds (CaO) ir neorganisks savienojums, kas satur jonu formās kalciju un skābekli (nedrīkst sajaukt ar kalcija peroksīdu, CaO).2). Pasaulē ir pazīstama kā kaļķis - vārds, kas apzīmē jebkuru neorganisku savienojumu, kas satur karbonātus, kalcija oksīdus un hidroksīdus, kā arī citus metālus, piemēram, silīciju, alumīniju un dzelzi..
Šis oksīds (vai kaļķis) arī tiek dēvēts par sarunvalodā kā bezkaļķaini vai sašķeltas kaļķi, atkarībā no tā, vai tas ir hidratēts. Kaļķi ir kalcija oksīds, savukārt kaļķainais kaļķis ir tā hidroksīds. Savukārt kaļķakmens (kaļķakmens vai rūdīts kaļķis) faktiski ir nogulumieži, kas sastāv galvenokārt no kalcija karbonāta (CaCO).3).

Tas ir viens no lielākajiem dabiskajiem kalcija avotiem un veido izejvielu kalcija oksīda ražošanai. Kā šis oksīds tiek ražots? Karbonāti ir jutīgi pret termisko sadalīšanos; kalcija karbonātu karsēšana temperatūrā virs 825 ° C, kas izraisa kaļķu un oglekļa dioksīda veidošanos.
Iepriekš minēto paziņojumu var aprakstīt šādi: CaCO3(s) → CaO (s) + CO2(g) Tā kā zemes garoza ir bagāta ar kaļķakmeni un kalcītu, un okeānos un pludmalēs ir bagātīgi jūras čaumalas (izejvielas kalcija oksīda ražošanai), kalcija oksīds ir salīdzinoši lēts reaģents..
Indekss
- 1 Formula
- 2 Struktūra
- 3 Rekvizīti
- 3.1. Šķīdība
- 4 Lietojumi
- 4.1. Kā javas
- 4.2. Brilles
- 4.3. Kalnrūpniecībā
- 4.4. Silikāta noņemšanas līdzeklis
- 5 Kalcija oksīda nanodaļiņas
- 6 Atsauces
Formula
Kalcija oksīda ķīmiskā formula ir CaO, kurā kalcijs ir līdzīgs skābes jonam (elektronu akceptoram) Ca2+, un skābekli kā pamata jonu (elektronu donoru) VAI2--.
Kāpēc kalcija ir +2 maksa? Tā kā kalcijs pieder periodiskās tabulas 2. grupai (Mr Becambara), un ir tikai divi valences elektroni, kas ir pieejami, lai veidotu saites, kas dod skābekļa atomu..
Struktūra
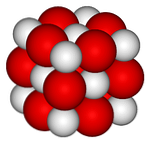
Augšējā attēlā ir attēlota kalcija oksīda kristāliskā struktūra (gem-salt type). Lielās sarkanās sfēras atbilst Ca joniem2+ un baltās sfēras ar joniem O2-.
Šajā kubiskā kristāla izkārtojumā katra jonu Ca2+ to ieskauj seši joni O2-, okluzē caurumi, ko atstāj lielie joni starp tiem.
Šī struktūra izsaka maksimālo šī oksīda jonu raksturu, lai gan ievērojamā rādiusu atšķirība (sarkanā sfēra ir lielāka par balto) piešķir vājāku kristālisko tīklenes enerģiju, salīdzinot ar MgO..
Rekvizīti
Fizikāli tas ir kristālisks balts ciets, bez smaržas un ar spēcīgu elektrostatisku mijiedarbību, kas ir atbildīgs par tās augstajiem kušanas punktiem (2572 ° C) un viršanu (2850 ° C). Turklāt tā molekulmasa ir 55,958 g / mol un interesanta īpašība ir termoluminiscējošs.
Tas nozīmē, ka kalcija oksīds, kas pakļauts liesmai, var spīdēt ar intensīvu baltu gaismu, kas angļu valodā pazīstams ar nosaukumu gaismu, vai spāņu valodā, kalcija gaisma. Ca joni2+, saskaroties ar uguni, tie rada sarkanīgu liesmu, kā parādīts nākamajā attēlā.

Šķīdība
CaO ir bāzes oksīds, kam ir spēcīga afinitāte pret ūdeni, ciktāl tā absorbē mitrumu (tā ir higroskopiska cieta viela), nekavējoties reaģējot uz sašķidrinātu kaļķi vai kalcija hidroksīdu:
CaO (s) + H2O (l) => Ca (OH)2(-i)
Šī reakcija ir eksotermiska (izdala siltumu), jo veidojas cieta viela ar spēcīgāku mijiedarbību un stabilāku kristāla režģi. Tomēr, ja Ca (OH) tiek uzsildīts, reakcija ir atgriezeniska2, to atūdeņo un apgaismo liepas; tad, kaļķis "atdzimis".
Iegūtais šķīdums ir ļoti vienkāršs, un, ja tas ir piesātināts ar kalcija oksīdu, tas sasniedz pH 12,8.
Tāpat tas ir šķīstošs glicerīnā un skābes un cukura šķīdumos. Tā kā tas ir bāzes oksīds, tam ir efektīva mijiedarbība ar skābes oksīdiem (SiO2, Al2O3 un Ticība2O3, piemēram) ir šķīstošs to šķidruma fāzēs. No otras puses, tas nešķīst spirtos un organiskajos šķīdinātājos.
Lietojumi
CaO ir daudz rūpnieciskas izmantošanas, kā arī acetilēna sintēzes (CH≡CH), fosfātu ekstrakcijā no notekūdeņiem un reakcijā ar sēra dioksīdu no gāzveida atkritumiem..
Citi kalcija oksīda izmantošanas veidi ir aprakstīti turpmāk:
Kā javas
Ja kalcija oksīds ir sajaukts ar smiltīm (SiO2) un ūdeni, kūkas ar smiltīm un lēni reaģē ar ūdeni, lai veidotos sašķeltas kaļķi. Savukārt CO2 no gaisa izšķīst ūdenī un reaģē ar sāli, veidojot kalcija karbonātu:
Ca (OH)2s) CO2(g) => CaCO3(s) + H2O (l)
CaCO3 Tas ir izturīgāks un cietāks savienojums nekā CaO, izraisot javu (iepriekšējo maisījumu) sacietēt un nostiprināt ķieģeļus, blokus vai keramiku starp tām vai vēlamo virsmu.
Stikla ražošanā
Būtiska izejviela brilles ražošanai ir silīcija oksīdi, kas sajaukti ar kaļķi, nātrija karbonātu (Na2CO3) un citām piedevām, pēc tam tos karsē, radot stiklotu cietu vielu. Pēc tam šo cieto vielu karsē un izsmidzina jebkuros skaitļos.
Ieguves rūpniecībā
Slāpēta kaļķi aizņem lielāku tilpumu nekā kārta, ko rada ūdeņraža saistīšanās (O-H-O) mijiedarbība. Šis īpašums tiek izmantots, lai izjauktu akmeņus no iekšpuses.
Tas tiek panākts, aizpildot tos ar kompaktu kaļķa un ūdens maisījumu, kas ir noslēgts, lai koncentrētu savu karstumu un ekspansīvo spēku klintī..
Kā silikāta noņemšanas līdzeklis
CaO ir sapludināts ar silikātiem, lai veidotu koalescējošu šķidrumu, ko pēc tam ekstrahē no konkrēta produkta izejvielas..
Piemēram, dzelzsrūda ir izejviela metāla dzelzs un tērauda ražošanai. Šie minerāli satur silikātus, kas ir nevēlami piemaisījumi procesam un tiek izvadīti ar tikko aprakstīto metodi.
Kalcija oksīda nanodaļiņas
Kalcija oksīdu var sintezēt kā nanodaļiņas, mainot kalcija nitrāta koncentrāciju (Ca (NO. \ T3)2) un nātrija hidroksīdu (NaOH) šķīdumā.
Šīs daļiņas ir sfēriskas, pamata (kā arī makro-mēroga cietā viela) un tām ir daudz virsmas. Līdz ar to šīs īpašības dod labumu katalītiskajiem procesiem. Kas? Pētījumi pašlaik atbild uz šo jautājumu.
Šīs nanodaļiņas tika izmantotas, lai sintezētu aizvietotus organiskos savienojumus, kas iegūti no piridīniem, jaunu zāļu formā, lai veiktu ķīmiskas transformācijas, piemēram, mākslīgo fotosintēzi, ūdens attīrīšanai no smagiem un kaitīgiem metāliem, un fotokatalītiskie līdzekļi.
Nanodaļiņas var sintezēt uz bioloģiskā atbalsta, piemēram, papaijas un zaļās tējas lapas, kas izmantojamas kā antibakteriāls līdzeklis..
Atsauces
- scifun.org (2018). Kaļķi: kalcija oksīds. Saturs iegūts 2018. gada 30. martā no: scifun.org.
- Vikipēdija. (2018). Kalcija oksīds. Saturs iegūts 2018. gada 30. martā no: en.wikipedia.org
- Ashwini Anantharaman et al. (2016). Zaļās kalcija oksīda nanodaļiņu un to pielietojumu sintēze. Inženierzinātņu pētniecības un pielietojuma žurnāls. ISSN: 2248-9622, 6. sējums, 10. izdevums, (-1. Daļa), 27.-31.
- J. Safaei-Ghomi et al. (2013). Kalcija oksīda nanodaļiņas katalizēja ļoti pakāpeniski aizvietotu piridīnu daudzpakāpju sintēzi etanola ūdens vidē Scientia Iranica, C darījumi: ķīmija un ķīmiskā tehnoloģija 20 549-554.
- PubChem. (2018). Kalcija oksīds. Saturs iegūts 2018. gada 30. martā no: pubchem.ncbi.nlm.nih.gov
- Shiver & Atkins. (2008). Neorganiskā ķīmija In 2. grupas elementi. (ceturtais izdevums, 280. lpp.). Mc Graw kalns.


