Alumīnija sulfīds (Al2S3) Ķīmiskā struktūra, nomenklatūra, īpašības
The alumīnija sulfīds (Al2S3) ir gaiši pelēks ķīmisks savienojums, ko veido metāliskā alumīnija oksidācija, zaudējot pēdējās enerģijas līmeņa elektronus un kļūstot par katjonu, un samazinot nemetālisko sēru, uzvarot alumīnija radītos elektronus un kļūstot par anjonu.
Lai tas notiktu, un alumīnija var dot savus elektronus, ir nepieciešams uzrādīt trīs hibrīda orbitālo sp3, kas dod iespēju veidot saites ar elektroniem no sēra.

Alumīnija sulfīda jutība pret ūdeni nozīmē, ka ūdens tvaiku klātbūtnē gaisā tā var reaģēt, lai iegūtu alumīnija hidroksīdu (Al (OH)).3), sērūdeņradis (H2S) un ūdeņradis (H2gāzveida; ja tas uzkrājas, tas var izraisīt eksploziju. Tāpēc alumīnija sulfīda iepakojums jāveic, izmantojot hermētiskus konteinerus.
No otras puses, tā kā alumīnija sulfīdam ir reaktivitāte ar ūdeni, tas padara to par elementu, kam nav šķīdības minētajā šķīdinātājā.
Indekss
- 1 Ķīmiskā struktūra
- 1.1. Molekulārā formula
- 1.2. Strukturālā formula
- 2 Rekvizīti
- 2.1 Fizikālās īpašības
- 2.2 Ķīmiskās īpašības
- 3 Lietojumi un lietojumprogrammas
- 3.1 Superkondensatoros
- 3.2. Sekundārajās litija baterijās
- 4 Riski
- 4.1 Pirmās palīdzības procedūra
- 4.2 Ugunsdzēsības pasākumi
- 5 Atsauces
Ķīmiskā struktūra
Molekulārā formula
Al2S3
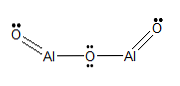
Strukturālā formula
- Alumīnija sulfīds.
- Di alumīnija trisulfīds.
- Alumīnija sulfīds (III).
- Alumīnija sulfīds.
Rekvizīti
Ķīmiskie savienojumi galvenokārt ir divu veidu īpašības: fizikāli un ķīmiski.
Fiziskās īpašības
Molārā masa
150,158 g / mol
Blīvums
2,02 g / ml
Kušanas punkts
1100 ° C
Šķīdība ūdenī
Nešķīstošs
Ķīmiskās īpašības
Viena no galvenajām alumīnija sulfīda reakcijām ir ūdens, substrāts vai galvenais reaģents:

Šajā reakcijā var novērot alumīnija hidroksīda un sērūdeņraža veidošanos, ja tas ir gāzes vai ūdeņraža sulfīda veidā, ja šķīdums tiek izšķīdināts ūdenī. Tās klātbūtni identificē sapuvušo olu smarža.
Lietojumi un lietojumprogrammas
Superkondensatoros
Alumīnija sulfīdu izmanto nano tīkla struktūru ražošanā, kas uzlabo īpatnējo virsmas laukumu un elektrisko vadītspēju tādā veidā, ka var sasniegt augstu kapacitāti un enerģijas blīvumu, kura pielietojamība ir tā, kas ir superkondensatoriem..
Grafēna oksīds (GO) - grafēns ir viens no allotropajiem oglekļa veidiem - tas ir kalpojis par atbalstu alumīnija sulfīdam (Al2S3) ar hierarhisku morfoloģiju, kas ir līdzīga nano-montanai, kas ražota, izmantojot hidrotermālu metodi.
Grafēna oksīda iedarbība
Grafēna oksīda īpašības kā balsts, kā arī augsta elektrovadītspēja un virsmas laukums padara nanorambutantu Al2S3 būt elektrochēmiski aktīviem.
CV specifiskas kapacitātes līknes ar labi definētiem redokspīķiem apstiprina nanorambutānu Al pseido-kapacitatīvo uzvedību2S3 hierarhiski, saglabājot grafēna oksīdu 1M NaOH elektrolītā. Specifiskās CV kapacitātes vērtības, kas iegūtas no līknēm, ir: 168,97 pie skenēšanas ātruma 5mV / s.
Turklāt ir novērots labs galvanostatiskais izlādes laiks 903 μs, liela īpatnējā kapacitāte 2178,16 pie strāvas blīvuma 3 mA / Cm.2. Enerģijas blīvums, kas aprēķināts no galvanostatiskās izlādes, ir 108,91 Wh / kg, strāvas blīvumam 3 mA / Cm2.
Tādējādi elektroķīmiskā pretestība apstiprina hierarhiskā nano-kolibra elektroda Al pseido-kapacitatīvo raksturu2S3. Elektroda stabilitātes tests uzrāda 57,44% īpašās kapacitātes saglabāšanu līdz 1000 cikliem.
Eksperimentālie rezultāti liecina, ka nanorambutants Al2S3 Hierarhisks ir piemērots supercapacitor lietojumiem.
Sekundārajās litija baterijās
Lai izstrādātu litija sekundāro akumulatoru ar augstu enerģijas blīvumu, alumīnija sulfīds (Al2S3) kā aktīvs materiāls.
Sākotnējā izlādes jauda, ko mēra no Al2S3 bija aptuveni 1170 mAh g-1 pie 100 mA g-1. Tas atbilst 62% no sēra teorētiskās jaudas.
Al2S3 ar nepietiekamu kapacitātes saglabāšanos potenciālajā diapazonā no 0,01 V līdz 2,0 V, galvenokārt, pateicoties uzlādes procesa vai Li ekstrakcijas strukturālajai neatgriezeniskumam..
XRD un K-XANES analīze par alumīniju un sēru liecināja, ka Al2S3 reaģē atgriezeniski iekraušanas un izkraušanas procesa laikā, bet Al kodols2S3 parādīja strukturālu neatgriezeniskumu, jo LiAl un Li2S veidojās no Al2S3 sākotnējā lejupielādē un pēc tam viņi palika tādi, kā tie bija.
Riski
- Saskarē ar ūdeni izdalās uzliesmojošas gāzes, kas spontāni var degt.
- Izraisa ādas kairinājumu.
- Izraisa nopietnu acu kairinājumu.
- Var izraisīt elpceļu kairinājumu.
Informācija var atšķirties atkarībā no piemaisījumiem, piedevām un citiem faktoriem.
Pirmās palīdzības procedūra
Vispārēja ārstēšana
Ja simptomi saglabājas, meklēt medicīnisko palīdzību.
Īpaša ārstēšana
Nav
Svarīgi simptomi
Nav
Ieelpošana
Ņem cietušo ārā. Sniedziet skābekli, ja ir grūti elpot.
Norīšana
Ievietot vienu vai divas glāzes ūdens un izraisīt vemšanu. Nekad neizraisiet vemšanu vai nesniedziet neko ar muti bezsamaņā.
Āda
Nomazgājiet skarto zonu ar ūdeni un vieglu ziepes. Noņemiet piesārņoto apģērbu.
Acis
Nomazgājiet acis ar ūdeni, bieži mirgo vairākas minūtes. Noņemiet kontaktlēcas, ja tādas ir, un turpiniet skalošanu.
Ugunsdzēsības pasākumi
Uzliesmojamība
Nav uzliesmojošs.
Ugunsdzēsības līdzekļi
Reaģē ar ūdeni. Nelietojiet ūdeni: izmantojiet CO2, smiltis un ugunsdzēšanas pulveri.
Cīņas procedūra
Izmantojiet pilnas sejas autonomu elpošanas aparātu ar pilnu aizsardzību. Valkāt apģērbu, lai izvairītos no saskares ar ādu un acīm.
Atsauces
- Salud y Riesgos.com, (s.f), Definīcija, jēdzieni un raksti par veselību, riskiem un vidi. Atgūts: saludyriesgos.com
- Alumīnija sulfīds. (s.f) Wikiwand. Saturs iegūts 2018. gada 9. martā: wikiwand.com
- Web elementi. (S.f) .Dialuminium Trisulpfide, atgūti 2018. gada 10. martā: webelements.com
- Iqbal, M., Hassan, M., M., Bibi.S., Parveen, B. (2017). Augstas īpatnējās jaudas un enerģijas blīvums sintezētā grafēna oksīda pamatā esošajam hierarhiskajam Al2S3 nanorambutānam, lietojot superkondensatoru lietošanai, Electrochimica Acta, 246. sējums ,Lappuses 1097-1103
- Senoh, H., Takeuchi, T., Hiroyuki K., Sakaebe, H., M., Nakanishi, K., Ohta, T., Sakai, T., Yasuda, K. (2010). Alumīnija sulfīda elektroķīmiskās īpašības lietošanai litijā.Enerģijas avotu žurnāls,195. sējums, 24. izdevums, Lapas 8327-8330 doi.org
- LTS Research Laboratories, Inc (2016), drošības datu lapa Alumīnija sulfīds: ltschem.com