Kalcija fosfāts (Ca3 (PO4) 2) struktūra, īpašības, veidošanās un izmantošana
The kalcija fosfāts ir neorganisks un terciārs sāls, kura ķīmiskā formula ir Ca3(PO4)2. Formula nosaka, ka šī sāls sastāvs kalcija un fosfāta gadījumā ir 3: 2. To var redzēt tieši apakšējā attēlā, kur redzama Ca cation2+ un anjonu PO43-. Par katru trīs Ca2+ Ir divi PO43- mijiedarbojas ar viņiem.
No otras puses, kalcija fosfāts attiecas uz virkni sāļu, kas atšķiras atkarībā no Ca / P attiecības, kā arī hidratācijas pakāpes un pH. Faktiski ir daudz veidu kalcija fosfāti, kas pastāv un ko var sintezēt. Tomēr pēc nomenklatūras burtiski kalcija fosfāts attiecas tikai uz iepriekš minēto trikalcija.

Visi kalcija fosfāti, ieskaitot Ca3(PO4)2, Tie ir cieti balti, ar nelieliem pelēcīgiem toņiem. Tās var būt granulētas, smalkas, kristāliskas un daļiņu izmēri ir aptuveni mikrometri; un pat ir sagatavoti šo fosfātu nanodaļiņas, ar kurām ir izstrādāti kaulu biokompetenti materiāli.
Šī bioloģiskā saderība ir saistīta ar to, ka šie sāļi ir atrodami zobos un, īsi sakot, zīdītāju kaulu audos. Piemēram, hidroksilapatīts ir kristālisks kalcija fosfāts, kas savukārt mijiedarbojas ar tā paša sāls amorfo fāzi..
Tas nozīmē, ka pastāv amorfi un kristāliski kalcija fosfāti. Šī iemesla dēļ daudzveidība un vairākas iespējas nav pārsteidzošas, ja sintezē materiālus, kuru pamatā ir kalcija fosfāti; materiāli, kuru īpašnieki katru dienu visā pasaulē ir ieinteresēti pievērsties kaulu atjaunošanai.
Indekss
- 1 Kalcija fosfāta struktūra
- 1.1 Amorfs kalcija fosfāts
- 1.2 Pārējā ģimene
- 2 Fizikālās un ķīmiskās īpašības
- 2.1 Nosaukumi
- 2.2. Molekulmasa
- 2.3. Fiziskais apraksts
- 2.4 Garša
- 2.5 Kušanas temperatūra
- 2.6. Šķīdība
- 2.7 Blīvums
- 2.8 Refrakcijas indekss
- 2.9. Standarta apmācības entalpija
- 2.10 Uzglabāšanas temperatūra
- 2,11 pH
- 3 Apmācība
- 3.1. Kalcija nitrāts un amonija hidrogēnfosfāts
- 3.2. Kalcija hidroksīds un fosforskābe
- 4 Lietojumi
- 4.1 Kaulu audos
- 4.2 Biokeramiskie cementi
- 4.3 Ārsti
- 4.4 Citi
- 5 Atsauces
Kalcija fosfāta struktūra
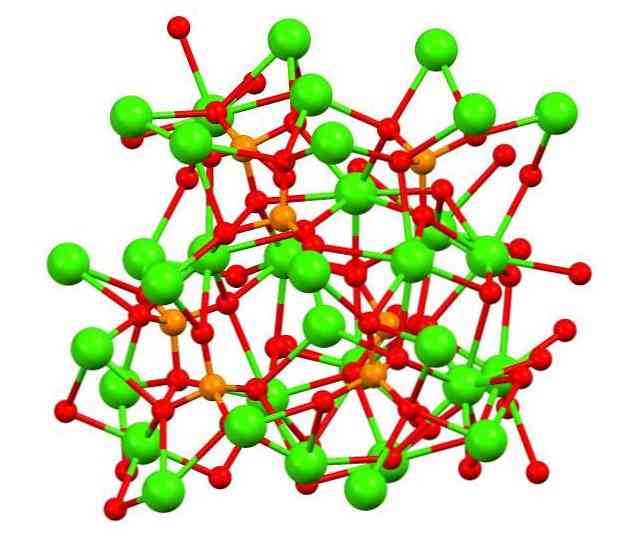
Augšējā attēlā parādīta tribīniskā kaliko fosfāta struktūra dīvainā baltā minerālvielā, kas var saturēt magniju un dzelzi kā piemaisījumus..
Lai gan no pirmā acu uzmetiena tas var šķist sarežģīts, ir jāprecizē, ka modelis pieņem kovalentās mijiedarbības starp fosfātu skābekļa atomiem un kalcija metāla centriem..
Pārstāvība ir derīga, tomēr mijiedarbība ir elektrostatiska; tas ir, katjoni Ca2+ ir piesaistīti PO anjoniem43- (Ca2+- O-PO33-). Paturot to prātā, saprotams, kāpēc attēlā kalciju (zaļās sfēras) ieskauj negatīvi uzlādēti skābekļa atomi (sarkanās sfēras).
Ja ir tik daudz jonu, tas neatstāj simetrisku izkārtojumu vai modeli. Ca3(PO4)2 Pieņem zemā temperatūrā (T<1000°C) una celda unitaria correspondiente a un sistema cristalino romboédrico; a este polimorfo se le conoce con el nombre de β-Ca3(PO4)2 (β-TCP, tā akronīms angļu valodā).
Augstās temperatūrās, no otras puses, tā tiek pārveidota par polimorfo α-Ca3(PO4)2 (α-TCP), kuras vienības šūna atbilst monoklīniskai kristāliskai sistēmai. Vēl augstākās temperatūrās var veidoties arī polimorfs α'-Ca3(PO4)2, kas ir sešstūra kristāla struktūra.
Amorfs kalcija fosfāts
Par kalcija fosfātu ir pieminētas kristāliskas struktūras, kuras sagaidāms no sāls. Tomēr tā spēj uzrādīt nesakārtotas un asimetriskas struktūras, kas vairāk saistītas ar "kalcija fosfāta stikla" tipu nekā kristāliem tā definīcijas izpratnē..
Kad tas notiek, tiek teikts, ka kalcija fosfātam ir amorfa struktūra (ĀKK, amorfs kalcija fosfāts). Vairāki autori norāda uz šāda veida struktūru, kas ir atbildīga par Ca bioloģiskajām īpašībām3(PO4)2 kaulu audos, tā remonts un biomimetizācija ir iespējama.
Noskaidrojot tās struktūru ar kodolmagnētiskās rezonanses (NMR) palīdzību, ir konstatēti OH jonu klātbūtne- un HPO42- ĀKK valstīs. Šie joni veidojas, hidrolizējot vienu no fosfātiem:
PO43- + H2O <=> HPO42- + OH-
Rezultātā ĀKK patiesā struktūra kļūst sarežģītāka, un tās jonu sastāvu attēlo formula: Ca9(PO4)6-x(HPO4)x(OH)x. "X" norāda hidratācijas pakāpi, jo, ja x = 1, tad formula būtu šāda: Ca9(PO4)5(HPO4) (OH).
Dažādas struktūras, ko PCA varēja būt atkarīgas no Ca / P molārā attiecība; tas ir, kalcija un fosfāta relatīvais daudzums, kas maina visu iegūto sastāvu.
Pārējā ģimene
Kalcija fosfāti faktiski ir neorganisko savienojumu grupa, kas savukārt var mijiedarboties ar organisko matricu.
Pārējos fosfātus iegūst "vienkārši", nomainot kalciju saturošos anjonus (PO43-, HPO42-, H2PO4-, OH-), kā arī piemaisījumu veidu cietā vielā. Tādējādi līdz vienpadsmit kalcija fosfātiem vai vairāk, katrs ar savu struktūru un īpašībām, var būt dabiski vai mākslīgi..
Zemāk ir daži fosfāti un to attiecīgās struktūras un ķīmiskās formulas:
-Ūdeņraža kalcija fosfāta dihidrāts, CaHPO4∙ 2H2O: monoklīnisks.
-Kalcija dihidrogēnfosfāta monohidrāts, Ca (H)2PO4)2∙ H2O: triklinika.
-Bezūdens dihidrogēnfosfāts, Ca (H)2PO4)2: triklinika.
-Okalcija hidrogēnfosfāts (OCP), Ca8H2(PO4)6: triklinika Tas ir hidroksilapatīta sintēzes prekursors.
-Hidroksapatīts, Ca5(PO4)3OH: sešstūris.
Fizikālās un ķīmiskās īpašības
Nosaukumi
-Kalcija fosfāts
-Trikalcija fosfāts
-Trikalcija difosfāts
Molekulmasa
310,74 g / mol.
Fiziskais apraksts
Tā ir bez smaržas balta cieta viela.
Garša
Garšīgs.
Kušanas punkts
1670 ° K (1391 ° C).
Šķīdība
-Praktiski nešķīst ūdenī.
-Nešķīst etanolā.
-Šķīst atšķaidītā sālsskābē un slāpekļskābē.
Blīvums
3,14 g / cm3.
Refrakcijas indekss
1,629
Standarta apmācības entalpija
4126 kcal / mol.
Uzglabāšanas temperatūra
2-8 ° C.
pH
6-8 kalcija fosfāta ūdens suspensijā ar 50 g / l.
Apmācība
Kalcija nitrāts un ūdeņraža amonija fosfāts
Kalcija fosfāta ražošanai vai veidošanai ir vairākas metodes. Viens no tiem sastāv no divu sāļu, Ca (NO), maisījuma.3)2∙ 4H2O un (NH4)2HPO4, iepriekš izšķīdināts absolūtā alkohola un ūdens daudzumā. Viens sāls nodrošina kalciju un citu fosfātu.
No šī maisījuma ĀKK nogulsnes, ko pēc tam karsē krāsnī 800 ° C un 2 stundas. Šīs procedūras rezultātā iegūst β-Ca3(PO4)2. Rūpīgi kontrolējot temperatūru, uzbudinājumu un saskares laiku, var rasties nanokristālu veidošanās.
Lai veidotu polimorfo-Ca3(PO4)2 ir nepieciešams sildīt fosfātu virs 1000 ° C. Šo sildīšanu veic citu metālu jonu klātbūtnē, kas stabilizē šo polimorfu, lai to varētu lietot istabas temperatūrā; tas ir, tas paliek stabilā metas stāvoklī.
Kalcija hidroksīds un fosforskābe
Kalcija fosfātu var veidot, sajaucot kalcija hidroksīda un fosforskābes šķīdumus ar neitralizāciju ar skābi. Pēc pusdienas nogatavināšanas mātes šķīdumos un to pienācīgas filtrēšanas, mazgāšanas, žāvēšanas un sijāšanas rezultātā tiek iegūts amorfā fosfāta granulēts pulveris..
Šī ĀKK reakcija rada augstu temperatūru, pārveidojoties saskaņā ar šādiem ķīmiskiem vienādojumiem:
2Ca9(HPO4) (PO4)5(OH) => 2Ca9(P2O7)0,5(PO4)5(OH) + H2O (pie T = 446,60 ° C)
2Ca9(P2O7)0,5(PO4)5(OH) => 3Ca3(PO4)2 + 0,5H2O (pie T = 748,56 ° C)
Šādā veidā iegūst β-Ca3(PO4)2, tās visizplatītākais un stabilākais polimorfs.
Lietojumi
Kaulu audos
Ca3(PO4)2 Tā ir galvenā kaulu pelnu neorganiskā sastāvdaļa. Tā ir kaulu aizvietotāju sastāvdaļa, kas izskaidrojama ar tās ķīmisko līdzību ar kaulā esošajām minerālvielām.
Kalcija fosfāta biomateriālus izmanto, lai labotu kaulu defektus un titāna metāla protēžu pārklājumu. Kalcija fosfāts tiek nogulsnēts uz tiem, izolējot tos no vides un palēninot titāna korozijas procesu.
Kalcija fosfāti, ieskaitot Ca3(PO4)2, Tos izmanto keramikas materiālu ražošanai. Šie materiāli ir bioloģiski saderīgi un pašlaik tiek izmantoti, lai atjaunotu alveolāro kaulu zudumu, ko izraisa periodonta slimība, endodontijas infekcijas un citi apstākļi..
Tomēr tos drīkst lietot tikai, lai paātrinātu periopisko kaulu remontu, vietās, kur nav hroniskas bakteriālas infekcijas.
Kalcija fosfātu var izmantot kaulu defektu labošanai, ja nav iespējams izmantot autogēnu kaulu transplantātu. Ir iespējams to lietot atsevišķi vai kopā ar bioloģiski noārdāmu un rezorbējošu polimēru, piemēram, poliglikolskābi..
Biokeramikas cementi
Kalcija fosfāta cements (CPC) ir vēl viens biokeramics, ko izmanto kaulu audu remontā. To ražo, sajaucot dažādu veidu kalcija fosfātu pulveri ar ūdeni, veidojot pasta. Pastu var injicēt vai pielāgot kaulu defektam vai dobumam.
Cementi tiek veidoti, pakāpeniski resorbēti un aizstāti ar tikko izveidotu kaulu.
Ārsti
-Ca3(PO4)2 Tas ir bāziskais sāls, tāpēc to lieto kā antacīdu, lai neitralizētu kuņģa skābes pārpalikumu un palielinātu pH. Zobu pastā tas nodrošina kalcija un fosfāta avotu, lai atvieglotu zobu un kaulu hemostāzes remineralizāciju..
-To izmanto arī kā uztura bagātinātāju, lai gan lētākais veids, kā aizstāt kalciju, ir tās karbonāta un citrāta izmantošana..
-Kalcija fosfātu var izmantot tetanīna, latentās hipokalcēmijas un uzturošās terapijas ārstēšanā. Turklāt tas ir noderīgs kalcija papildināšanai grūtniecības un zīdīšanas laikā.
-To izmanto piesārņojuma ārstēšanai ar radioaktīvo izotopu radio (Ra-226) un stroncija (Sr-90). Kalcija fosfāts bloķē radioaktīvo izotopu absorbciju gremošanas traktā, tādējādi ierobežojot to radīto kaitējumu.
Citi
-Kalcija fosfāts tiek izmantots kā putnu barība. Turklāt to izmanto zobu pastās, lai kontrolētu zobakmens.
-To lieto kā pretsalipes līdzekli, piemēram, lai nepieļautu sāls saspiešanu.
-Tas darbojas kā balināšanas līdzeklis miltiem. Kaut gan cūkgaļas cūciņa novērš nevēlamu krāsu un uzlabo cepšanas stāvokli.
Atsauces
- Tung M.S. (1998) Kalcija fosfāti: struktūra, sastāvs, šķīdība un stabilitāte. In: Amjad Z. (eds) Kalcija fosfāti bioloģiskajās un rūpnieciskajās sistēmās. Springer, Boston, MA.
- Langlang Liu, Yanzeng Wu, Chao Xu, Suchun Yu, Xiaopei Wu un Honglian Dai. (2018). "Nano-β-trikalcija fosfāta un inhibēšanas hepatocelulārās karcinomas šūnās sintēze, raksturojums", Journal of Nanomaterials, vol. 2018, 7083416., 7 lappuses, 2018. gads.
- Ķemmes, Kristus un Reijs, kristietis. (2010). Amorfs kalcija fosfāts: sintēze, īpašības un izmantošana biomateriālos. Acta Biomaterialia, vol. 6 (Nr. 9). pp. 3362-3378. ISSN 1742-7061
- Vikipēdija. (2019). Trikalcija fosfāts. Saturs iegūts no: en.wikipedia.org
- Abida et al. (2017). Trikalcija fosfāta pulveris: sagatavošanas, raksturošanas un blīvēšanas spējas. Vidusjūras žurnāls Chemistry 2017, 6 (3), 71-76.
- PubChem. (2019). Kalcija fosfāts. Saturs iegūts no: pubchem.ncbi.nlm.nih.gov
- Elsevier (2019). Kalcija fosfāts. Science Direct. Saturs iegūts no: sciencedirect.com


