Nātrija hlorīda (NaCl) struktūra, īpašības, izmantošana, toksicitāte
The nātrija hlorīds, sauc arī par parasto sāli vai galda sāli, ir sārmu metālu nātrija un halogēna hlora binārais neorganiskais sāls. Tas ir lielākais ēdamās sāls komponents, un tā minerālviela ir pazīstama kā halīts. Tās molekulārā formula ir NaCl, un apraksta tās jonu stehiometrisko attiecību (Na+ Cl-), nevis diskrēta molekula (Na-Cl)
Nātrija hlorīds ir kristāliska balta cieta viela, ko veido nātrija, sudrabaini baltā metāla kombinācija, kas stipri reaģē ar ūdeni, un hlora elements, indīgs, kodīgs, gaiši zaļš gāze.

Augšējā attēlā parādīta daļa NaCl kristālu. Kā ir iespējams, ka divi elementi ir tikpat bīstami kā Na un Cl2, var veidoties ēdams sāls? Pirmkārt, tā veidošanās ķīmiskais vienādojums ir:
2Na (s) + Cl2(g) => 2NCl (s)
Atbilde ir saistīta ar saikni NaCl. Tā ir jonu īpašības, Na+ un Cl- tie ir diagonāli atšķirīgi no neitrālo atomu.
Nātrija ir būtisks elements, bet tā jonu forma. Na+ ir galvenais ekstracelulārais katjons, kura koncentrācija ir aptuveni 140 mEq / lt, un kopā ar papildu anjoniem, Cl- un HCO3- (bikarbonāts), galvenokārt ir atbildīgas par osmolaritātes un ekstracelulārā tilpuma vērtību.
Turklāt Na+ ir atbildīgs par nervu impulsu rašanos un vadīšanu neironu asīs, kā arī par muskuļu kontrakcijas uzsākšanu.
NaCl ir izmantots kopš seniem laikiem, lai garšotu pārtiku un saglabātu gaļu, jo tā spēj likvidēt baktērijas un novērst bojājumus.
Tas ir nepieciešams arī nātrija hidroksīda (NaOH) un molekulārā hlora (Cl2), NaCl reaģējot ar hidrolīzes ūdeni: \ t
2H2O (l) + 2 NaCl (s) => 2NaOH (ac) + Cl2(g) + H2(g)
Katodā (-) H uzkrājas2 (g) un NaOH. Tikmēr Cl uzkrājas anodā (+)2 (g) Nātrija hidroksīdu izmanto ziepju un hlora ražošanā PVC plastmasas ražošanā.
Indekss
- 1 Nātrija hlorīda struktūra
- 1.1. Vienota šūna
- 2 Rekvizīti
- 2.1. Molekulārā formula
- 2.2. Molekulmasa
- 2.3. Fiziskais apraksts
- 2.4 Krāsa
- 2.5 Garša
- 2.6 Viršanas punkts
- 2.7. Kušanas punkts
- 2.8 Šķīdība ūdenī
- 2.9 Šķīdība organiskos šķīdinātājos
- 2.10. Blīvums
- 2.11. Tvaika spiediens
- 2.12 Stabilitāte
- 2.13 Sadalīšanās
- 2.14 Viskozitāte
- 2.15 Korozija
- 2,16 pH
- 3 Lietojumi
- 3.1 Pārtikas produktos
- 3.2. Rūpnieciskā izmantošana
- 3.3. Mājās
- 3.4 Citi izmantošanas veidi
- 3.5 Terapeitiskie lietojumi
- 4 Toksicitāte
- 4.1 Norīšana
- 4.2 Kairinājums un fiziska saskare
- 5 Atsauces
Nātrija hlorīda struktūra
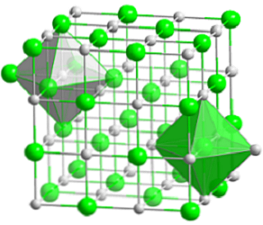
Augšējā attēlā ir attēlota nātrija hlorīda kompakta kubiskā struktūra. Lielās zaļās sfēras atbilst Cl anjoniem-, baltā krāsā, uz Na katjoniem+. Ņemiet vērā, kā NaCl kristāls sastāv no jonu tīkla, kas sakārtots pēc to elektrostatiskās mijiedarbības ar attiecību 1: 1.
Lai gan attēlā ir attēloti stieņi, saites nav kovalentās, bet jonu. Stieņu izmantošana ir noderīga, kad tiek rādīta koordinācija ģeometrija ap jonu. Piemēram, NaCl gadījumā katra Na+ to ieskauj seši Cl- (balta oktahedrera) un katra Cl- sešas Na+ (zaļš oktaedrs).
Tāpēc tai ir koordinācija (6,6), kuras skaitļi norāda, cik kaimiņi ieskauj katru jonu. Numurs labajā pusē norāda Na kaimiņus+, kamēr kreisajā pusē - Cl-.
Citos attēlos nav izmantoti stieņi, lai izceltu oktaedrālos caurumus, ko struktūra ir, kas izriet no starpstarpu telpas starp sešiem Cl anjoniem.- (vai Na katjoni+) iepakotas. Šo kārtību novēro citos mono (MX) vai poliatomātiskos neorganiskos sāļos, un to sauc par gem sāli..
Vienota šūna
Akmens sāls vienības šūna ir kubiskā, bet kuras kubi tieši attēlo iepriekš attēlā? Oktaedri sniedz atbildi. Abi pārklāj četrus mazus kubus.
Šiem kubiem ir daļu no joniem to virsotnēs, malās un sejās. Rūpīgi novērojot jonu Na+ tā atrodas centrā un divpadsmit no tiem malās. Jonu vienā malā var koplietot četri kubi. Tātad ir 4 Na joni+ (12 × 1/4 + 1 = 4).
Cl joniem-, astoņi atrodas virsotnēs un sešās malās. Tā kā joniem, kas novietoti pie virsotnēm, ir telpa ar astoņiem citiem kubiem, un malās ar sešiem, tiem ir 4 Cl joni- (8 × 1/8 + 6 × 1/2 = 4).
Iepriekšējo rezultātu interpretē šādi: NaCl vienības šūnā ir četri Na katjoni+ un četri Cl anjoni-; proporcija, kas atbilst ķīmiskajai formulai (Na+ katram Cl-).
Rekvizīti
Molekulārā formula
NaCl.
Molekulmasa
58,44 g / mol.
Fiziskais apraksts
Kristāliska cieta viela.
Krāsa
Caurspīdīgi, bezkrāsaini kristāli vai balts kristālisks pulveris.
Garša
Sāļš.
Viršanas punkts
2,575 ° F līdz 760 mmHg.
1465 ° C.
Kušanas punkts
1,474 ° F (800,7 ° C).
Gan viršanas punkts, gan kausēšanas temperatūra atspoguļo siltumu, kas nepieciešams, lai pārvarētu kristālisko tīklenes enerģiju. Tāpēc šie mērījumi apstiprina NaCl jonu raksturu.
Šķīdība ūdenī
Lielāks vai vienāds ar 100 mg / ml 68 ° F temperatūrā.
36,0 g / 100 ml 25 ° C temperatūrā.
Faktiski tas ir higroskopisks sāls, kas saglabā mitrumu no vides.
Šķīdība organiskos šķīdinātājos
0,065 g / 100 ml etanola 25 ° C temperatūrā; 10 g / 100 g glicerīna 25 ° C temperatūrā; 2,15 g / 100 ml šķidrā amonija 40 ° C temperatūrā; 1,4 g / 100 ml metanola 25 ° C temperatūrā; 7,15 g / 100 etilēnglikola 25 ° C temperatūrā un 5,21 g / 100 g skudrskābes 25 ° C temperatūrā.
Blīvums
2,165 g / cm3 pie 77 ° C.
Tvaika spiediens
1 mmHg līdz 1,589 ° F.
Stabilitāte
Tas ir stabils ieteicamajos uzglabāšanas apstākļos.
Sadalīšanās
Sildot uz augstām temperatūrām, tā sadalās, izdalot sālsskābes un dinātrija oksīda tvaikus.
Viskozitāte
Piesātināto šķīdumu viskozitāte 1,93 mPa-s.
Korozija
Tas ir kodīgs daudziem metāliem.
pH
6.7 līdz 7.3 ūdenī.
Lietojumi
Pārtikas produktos
-Nātrija hlorīds kopš seniem laikiem ir izmantots, lai uzlabotu pārtikas garšu un tā saglabāšanu. Gaļas sālīšana ir veids, kā to saglabāt no baktēriju darbības, jo tas aizkavē proteīnu sadalīšanos.
-No otras puses, sāls palielina osmolaritāti ap gaļu, kas izraisa osmozes absorbciju baktēriju ūdenī, kas izraisa tās izvadīšanu..
Rūpnieciskais pielietojums
Pārtikas rūpniecība
-Pārtikas rūpniecībā sāls tiek izmantots kā garšas pastiprinātājs, fermentācijas kontroles piedeva, tekstūras kontroles līdzeklis un krāsu attīstītājs. Piemēram, pievieno sāli, lai izceltu krāsu bekonā, šķiņķī un citos gaļas produktos.
-Sāls kalpo kā saistviela desu ražošanā. Tas veicina saistvielas gela veidošanos, kas sastāv no gaļas, taukiem un mitruma.
-Apstrādājot miltus maizes ražošanā, vārīšanas laikā pievieno sāli, lai kontrolētu maizes mīklas fermentācijas ātrumu. To izmanto arī, lai stiprinātu lipekli un kā garšas pastiprinātāju, kā arī ceptu produktu pildījumu.
-To lieto brokastu graudu ražošanā, jauktos vai sagatavotos miltos, frī kartupeļos, ēdienos suņiem un kaķiem utt..
Ķīmisko produktu sintēze
-Nātrija hlorīds tiek izmantots kā izejviela nātrija hidroksīda un hlora ražošanā, kas savukārt ir noderīga daudzās ķīmiskās rūpniecības nozarēs..
-Sāls tiek izmantots dažādu metālu, piemēram, alumīnija, vara, tērauda un vanādija, apstrādē. To izmanto arī, lai pagatavotu nātrija hlorātu, ko pēc tam izmanto hlora dioksīda sintēzes procesā, kas ir skābekļa bāzes balinātājs. Hlora dioksīds ir mazāk kaitīgs videi nekā citi balinātāji.
Ādas rūpniecībā
-Sāls tiek izmantots, lai aizkavētu baktēriju darbību ādas iekšpusē, kā arī palīdzētu tās rehidratācijā.
Tekstilrūpniecībā
-Sāls tiek izmantots kā auduma krāsošanas līdzeklis. To izmanto kā sālsūdens skalošanas līdzekli, lai izņemtu organiskos piesārņotājus un radītu pozitīvu lādiņu uz audumu virsmas, kas ļauj savienot negatīvi uzlādētās krāsvielas..
Naftas rūpniecībā
-Naftas un gāzes izpētē sāls ir svarīga urbšanas šķidrumu sastāvdaļa. To izmanto, lai flokulētu un palielinātu urbšanas šķidrumu blīvumu, kas ļauj pārvarēt gāzes augsto spiedienu sasniedzamajās akās. Turklāt sāls saglabā urbšanas šķidruma piesātinājumu.
-Sāls palīdz kompakto augsni, uz kuras ceļi būvēti. Samazina zemūdens novirzi, mainot mitrumu un automobiļu satiksmi.
Mājās
Sāls ir izmantots, berzējot virsmu, podiņu un pannu tīrīšanu. Arī pelējuma profilaksei un traipu noņemšanai. To izmanto arī daudzos šampūnu un zobu pastu zīmolos.
Citi izmantošanas veidi
Uz ceļiem
-Gaidot sniegputenus, ceļi ir klāti ar sālījumu, kas novērš ledus savienošanos ar ceļa virsmu. Atkausēšanai tiek izmantots sāls un sāls maisījums, un dažreiz tiek pievienoti citi ķīmiskie komponenti, piemēram, magnija vai kalcija hlorīdi. Sāls un sāls šķīdums nav efektīvs temperatūrā, kas zemāka par -10ºC.
Pievienojot sāli, samazinās krioskopiskais punkts, risinājumu koligatīvais īpašums, kas zināmā mērā kavē ledus veidošanos..
-Higroskopiskā stāvokļa dēļ sāls tiek izmantots kā lēts desikants.
Ūdens mīkstināšanai izmantotajos sveķos
Cietais ūdens satur kalcija un magnija jonus, kas kavē ziepju iedarbību un ražo sārmainā materiāla nogulsnes dažādās iekārtās un caurulēs. Ūdens mīkstināšanas procesā tiek izmantoti jonu apmaiņas sveķi. Sāls tiek izmantots sveķu sagatavošanā un reģenerācijā.
Uz ugunsdzēšamajiem aparātiem
Ugunsdzēšamajos aparātos izmanto nātrija hlorīdu, lai cīnītos pret ugunsgrēkiem, kuros ir degoši metāli, piemēram, magnija, kālija, nātrija un NK sakausējumi..
Sāls darbojas kā siltuma izlietne, kā arī kā drupinātājs, kas ierobežo skābekļa piekļuvi ugunsgrēkam.
Brilles
Nātrija hlorīda kristāli tiek izmantoti optiskos komponentos, piemēram, logos un prizmās, īpaši infrasarkanajā gaismā. Tomēr, tā kā sāls ir ļoti higroskopisks, rodas kāda veida sala, kas aptver lēcas. Šī iemesla dēļ nātrija hlorīda lēcas ir aizstātas ar cinka selenīda (ZnSe) lēcām..
Terapeitiskie lietojumi
Papildināt sāļu trūkumu organismā
-Kad ir Na organisma izsīkums+, jāaizstāj, lai saglabātu ekstracelulāro osmolaritāti, nervu vadīšanu un muskuļu kontrakciju.
-NaCl lieto nātrija un hlora deficīta ārstēšanai un profilaksei, ko izraisa pārmērīga svīšana augsta temperatūras iedarbības laikā. To lieto arī pārmērīgas diurēzes vai pārmērīga sāls patēriņa ierobežojuma gadījumā.
-045% NaCl šķīduma parenterālu ievadīšanu izmanto hiperosmolārā diabēta ārstēšanai. Tā pilda rehidratācijas funkciju un palīdz novērtēt nieru funkcijas stāvokli.
-Hipertonisku šķīdumu injicēšana ar NaCl koncentrāciju, kas lielāka par 0,9%,
-Tos lieto, ja ir smaga Na+, būtiskas jonu atjaunošana. Šī hiponatriēmija var būt ārstēšanās ar brīviem elektrolītiem vai Na koncentrācija+.
Hiponatriēmiju var izraisīt arī pārmērīga ūdens uzņemšana, ko nekontrolē nepietiekama nieru darbība.
Procedūrās un netradicionālos lietojumos
-NaCl inhalācijas šķīdumi tiek izmantoti, lai atšķaidītu miglošanas procesā izmantotās zāles. To izmanto arī trahejas mazgāšanai un apūdeņošanai. 0,9% sāls šķīdums, ko lieto deguna aerosolos.
-20% NaCl šķīdumu lieto intra-amnionālai transabdominālai instalācijai, tādējādi izraisot vēlu abortu grūtniecības otrajā trimestrī.
-Nātrija hlorīdu var izmantot kā vietēju antiseptisku līdzekli. Pateicoties tās osmotiskajai spējai, tā spēj dehidratēt plašu vīrusu un baktēriju spektru nesadegušā stāvoklī; tāpēc to lieto kā sāpīgu antiseptisku līdzekli brūču dezinficēšanai.
Toksicitāte
Norīšana
Tam ir tikai kaitīga ietekme uz veselību, ja uzņemšana ir augsta un ilgstoša. Šādos apstākļos hipernatriēmija rastos, palielinoties ekstracelulārajam tilpumam, kas varētu izraisīt augstu asinsspiedienu.
Kairinājums un fizisks kontakts
Tam ir toksiska iedarbība tikai tad, ja ieelpošana ir ļoti augsta. Saskaroties ar ādu pārmērīgi, tas var izraisīt sausumu. Visbeidzot, tas saskarē ar acīm izraisa īslaicīgu kairinājumu.
Atsauces
- Shiver & Atkins. (2008). Neorganiskā ķīmija (Ceturtais izdevums, 84., 90., 93., 263. lpp.). Mc Graw kalns.
- Whitten, Davis, Peck & Stanley. Ķīmija (8. izdevums). CENGAGE Learning, 482-483. Lpp.
- Nātrija hlorīds (2018). Nātrija hlorīds: ieguvumi, lietošanas veidi, īpašības, riski. Uzņemts no: clorurodesodio.org
- PubChem. (2018). Nātrija hlorīds. Saturs iegūts no: pubchem.ncbi.nlm.nih.gov
- Vikipēdija. (2018). Nātrija hlorīds. Uzņemts no: en.wikipedia.org
- Amerikāņu elementi. (2018). Nātrija hlorīds. Ievesta no: americanelements.com


