Etilacetāta struktūra, īpašības, sintēze, lietošanas veidi un riski
The etilacetātu vai etiletanoātu (IUPAC nosaukums) ir organisks savienojums, kura ķīmiskā formula ir CH3COOC2H5. Tas sastāv no estera, kur spirta komponents ir iegūts no etanola, bet tā karboksilskābes sastāvdaļa ir no etiķskābes.
Tas ir šķidrums normālos temperatūras un spiediena apstākļos, kas rada patīkamu aromātu augļiem. Šis īpašums ir ideāli saskaņots ar to, kas tiek gaidīts no estera; kas ir faktiski etilacetāta ķīmiskais raksturs. Šā iemesla dēļ tā izmanto pārtiku un alkoholiskos dzērienus.
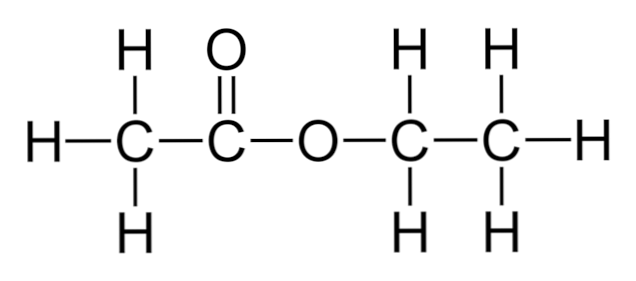
Augšējā attēlā ir parādīts etilacetāta konstrukcijas karkass. Pievērsiet uzmanību kreisajam tās karboksilskābes komponentam un pa labi no spirta komponenta. No strukturālā viedokļa varētu sagaidīt, ka šis savienojums darbojas kā hibrīds starp etiķi un alkoholu; tomēr tam piemīt savas īpašības.
Šādi hibrīdi, ko sauc par esteri, izceļas kā atšķirīgi. Etilacetāts nevar reaģēt kā skābe, kā arī nevar dehidrēt, ja nav OH grupas. Tā vietā tas tiek pakļauts pamata hidrolīzei spēcīgas bāzes, piemēram, nātrija hidroksīda, NaOH klātbūtnē.
Šī hidrolīzes reakcija tiek izmantota mācību laboratorijās ķīmisko eksperimentu veikšanai; turklāt reakcija ir otrās kārtas. Kad notiek hidrolīze, praktiski etiletanoāts atgriežas sākotnējās sastāvdaļās: skābe (deprotonēta ar NaOH) un alkohols..
Savā strukturālajā skeletā konstatēts, ka ūdeņraža atomi dominē pār skābekli. Tas ietekmē viņu spēju mijiedarboties ar tādām sugām, kas nav polāri, piemēram, taukiem. To lieto arī tādu savienojumu, kā sveķi, krāsvielas un vispārīgi organiskas vielas, izšķīdināšanai.
Neskatoties uz patīkamu aromātu, ilgstoša šīs šķidruma iedarbība rada negatīvu ietekmi (tāpat kā gandrīz visus ķīmiskos savienojumus) organismā.
Indekss
- 1 etilacetāta struktūra
- 1.1 Ūdeņraža donoru atomu neesamība
- 2 Fizikālās un ķīmiskās īpašības
- 2.1 Nosaukumi
- 2.2 Molekulārā formula
- 2.3. Molekulmasa
- 2.4. Fiziskais apraksts
- 2.5 Krāsa
- 2.6 Smarža
- 2.7 Garša
- 2.8 Smaržas slieksnis
- 2.9 Viršanas punkts
- 2.10 Kušanas punkts
- 2.11 Šķīdība ūdenī
- 2.12 Šķīdība organiskos šķīdinātājos
- 2.13 Blīvums
- 2.14 Tvaika blīvums
- 2.15 Stabilitāte
- 2.16. Tvaika spiediens
- 2.17 Viskozitāte
- 2.18 Degšanas siltums
- 2.19 Iztvaikošanas siltums
- 2.20 Virsmas spriedze
- 2.21 Refrakcijas indekss
- 2.22 Uzglabāšanas temperatūra
- 2.23 pKa
- 3 Kopsavilkums
- 3.1 Zvejas reakcija
- 3.2 Tishchenko reakcija
- 3.3 Citas metodes
- 4 Lietojumi
- 4.1 Šķīdinātājs
- 4.2 Mākslīgie aromāti
- 4.3 Analītika
- 4.4. Organiskā sintēze
- 4.5. Hromatogrāfija
- 4.6. Entomoloģija
- 5 Riski
- 6 Atsauces
Etilacetāta struktūra
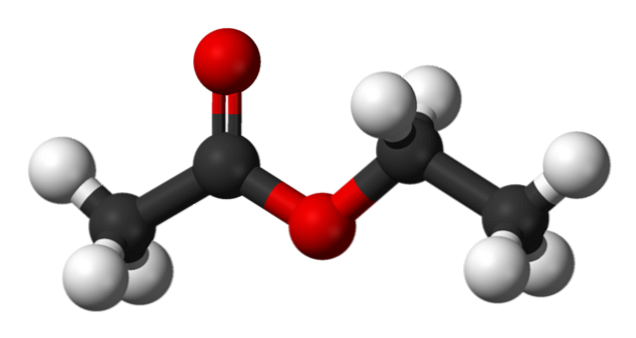
Augšējā attēlā etilacetāta struktūra ir attēlota ar sfēru un stieņu modeli. Šajā modelī tiek izcelti skābekļa atomi ar sarkanām sfērām; kreisajā pusē ir frakcija, kas iegūta no skābes, un labajā pusē ir frakcija, kas iegūta no spirta (alkoksigrupa, -OR)..
Karbonilgrupu novērtē C = O saite (dubultstieņi). Konstrukcija ap šo grupu un blakus esošo skābekli ir plakana, jo pastāv slodzes pārvietošana no rezonanses starp abiem oksigeniem; fakts, kas izskaidro α-hidrogēnu salīdzinoši zemo skābumu (-CH grupas skābumu)3, saistīts ar C = O).
Molekula, rotējot divas tās saites, tieši atbalsta to, kā tā mijiedarbojas ar citām molekulām. Divu skābekļa atomu klātbūtne un struktūras asimetrija dod tai pastāvīgu dipola momentu; kas savukārt atbild par dipola-dipola mijiedarbību.
Piemēram, elektroniskais blīvums ir lielāks pie diviem skābekļa atomiem, ievērojami samazinoties grupā -CH3, un pakāpeniski OCH grupā2CH3.
Šo mijiedarbību dēļ etilacetāta molekulas normālos apstākļos veido šķidrumu, kuram ir ievērojami augsts viršanas punkts (77 ° C)..
Nav ūdeņraža saites donoru atomu
Ja jūs uzmanīgi skatāties uz struktūru, jūs pamanīsiet, ka nav atoma, kas spēj ziedot ūdeņraža tiltu. Tomēr skābekļa atomi ir tādi akceptori, un etilacetāts ūdenī ir ļoti labi šķīstošs un ievērojami ietekmē mijiedarbību ar polāriem savienojumiem un ūdeņraža saiti donoriem (piemēram, cukuriem)..
Tas arī ļauj jums lieliski sadarboties ar etanolu; tāpēc tās klātbūtne alkoholiskajos dzērienos nav pārsteidzoša.
No otras puses, tā alkoksigrupa padara to spējīgu mijiedarboties ar dažiem apolāriem savienojumiem, piemēram, hloroformu, CH3Cl.
Fizikālās un ķīmiskās īpašības
Nosaukumi
-Etilacetāts
-Etiletanoāts
-Etiķskābes esteris
-Acetoksietāns
Molekulārā formula
C4H8O2 vai CH3COOC2H5
Molekulmasa
88,106 g / mol.
Fiziskais apraksts
Dzidrs, bezkrāsains šķidrums.
Krāsa
Bezkrāsains šķidrums.
Smarža
Raksturīgi ēteriem, līdzīgi ananāsu smaržai.
Garša
Patīkams, kad atšķaidīts, pievieno alus augļu garšu.
Smaržas slieksnis
3,9 ppm. 0,0196 mg / m3 (zema smaka); 665 mg / m3 (augsta smarža).
Nosakāms smarža 7 - 50 ppm (vidējais = 8 ppm).
Viršanas punkts
171 ° F līdz 760 mmHg (77,1 ° C).
Kušanas punkts
-118,5 ° F (-83,8 ° C).
Šķīdība ūdenī
80 g / l.
Šķīdība organiskos šķīdinātājos
Sajaucas ar etanolu un etilēteri. Ļoti labi šķīst acetonā un benzolā. Samaisāms arī ar hloroformu, fiksētām un gaistošām eļļām, kā arī ar skābekli un hlorētiem šķīdinātājiem.
Blīvums
0,9003 g / cm3.
Tvaika blīvums
3.04 (gaisa attiecība: 1).
Stabilitāte
Tas lēnām sadalās ar mitrumu; nesaderīgs ar vairākām plastmasām un stipriem oksidētājiem. Maisījums ar ūdeni var būt sprādzienbīstams.
Tvaika spiediens
93,2 mmHg pie 25 ° C
Viskozitāte
0,423 mPoise pie 25 ° C.
Degšanas siltums
2,238,1 kJ / mol.
Iztvaikošanas siltums
35,60 kJ / mol 25 ° C temperatūrā.
Virsmas spriedze
24 din / cm pie 20 ° C.
Refrakcijas indekss
1,373 pie 20 ° C / D.
Uzglabāšanas temperatūra
2 - 8 ° C.
pKa
16 - 18 ° C temperatūrā.
Sintēze
Fišera reakcija
Etilacetātu rūpnieciski sintezē ar Fisher reakciju, kurā etanols tiek esterificēts ar etiķskābi. Reakcija tiek veikta istabas temperatūrā.
CH3CH2OH + CH3COOH <=> CH3COOCH2CH3 + H2O
Reakciju paātrina ar skābes katalīzi. Līdzsvara virzība pa labi, tas ir, pret etilacetāta ražošanu, noņemot ūdeni; saskaņā ar Masu rīcības likumu.
Tishchenko reakcija
Etilacetātu ražo arī rūpnieciski, izmantojot Tishchenko reakciju, konjugējot divus ekvivalentus acetaldehīda ar alkoksīda izmantošanu kā katalizatoru..
2 CH3CHO => CH3COOCH2CH3
Citas metodes
-Etilacetātu sintezē kā kopproduktu butāna oksidēšanā etiķskābē reakcijā, kas tiek veikta 175 ° C un 50 atm spiediena temperatūrā. Kobalta un hroma jonus izmanto kā katalizatoru.
-Etilacetāts ir polivinilacetāta etanolīzes līdz polivinilspirta produkts.
-Etilacetātu ražo arī rūpniecībā ar etanola dehidrogenēšanu, un reakciju katalizē vara lietošana paaugstinātā temperatūrā, bet zemāka par 250 ° C..
Lietojumi
Šķīdinātājs
Etilacetātu izmanto kā šķīdinātāju un atšķaidītāju, ko izmanto ķēdes plātņu tīrīšanā. To izmanto kā šķīdinātāju modificēta apiņu ekstrakta ražošanā, kā arī kafijas un tējas lapu kofeīna ražošanā. To izmanto tintēs, ko izmanto, lai atzīmētu augļus un dārzeņus.
Etilacetātu izmanto tekstilrūpniecībā kā tīrīšanas līdzekli. To lieto termometru kalibrēšanā, ko izmanto cukuru atdalīšanai. Krāsas rūpniecībā to izmanto kā šķīdinātāju un izmantoto materiālu atšķaidītāju.
Mākslīgie aromāti
To izmanto augļu garšu izstrādē; Piemēram: banānu, bumbieru, persiku un ananāsu, kā arī vīnogu aromātu utt..
Analytics
To izmanto bismuta, bora, zelta, molibdēna un platīna, kā arī tallija šķīdinātāja noteikšanai. Etilacetātam ir iespēja iegūt daudzus savienojumus un elementus ūdens šķīdumā, piemēram, fosforu, kobaltu, volframu un arsēnu.
Organiskās sintēzes
Etilacetātu izmanto rūpniecībā kā viskozitātes samazināšanas līdzekli sveķiem, ko izmanto fotorezistīvos preparātos. To lieto acetamīda, acetilacetāta un metil heptanona ražošanā.
Hromatogrāfija
Laboratorijās kā kolonnu hromatogrāfiju un ekstrakcijas šķīdinātāju izmanto etilacetātu. Ar etilacetātu salīdzinoši zemu viršanas temperatūru ir viegli iztvaicēt, kas ļauj izšķīdinātās vielas koncentrēt šķīdinātājā..
Entomoloģija
Etilacetātu lieto entomoloģijā, lai apslāpētu kukaiņus, kas ievietoti traukā, kas ļauj to savākt un pētīt. Etilacetāta tvaiki iznīcina kukaiņu, neiznīcinot to un novēršot tās sacietēšanu, atvieglojot tā montāžu savākšanai.
Riski
-LD50 etilacetāta koncentrācija žurkām norāda uz zemu toksicitāti. Tomēr tas var kairināt ādu, acis, ādu, degunu un rīkles.
-Augsta līmeņa iedarbība var izraisīt reiboni un ģīboni. Arī ilgstoša iedarbība var ietekmēt aknas un nieres.
-Etilacetāta ieelpošana ar koncentrāciju 20 000 - 43 000 ppm var izraisīt plaušu tūsku un asiņošanu.
-Arodekspozīcijas robežvērtību OSHA ir noteikusi 400 ppm gaisā vidēji 8 stundu darba maiņas laikā.
Atsauces
- Steven A. Hardinger. (2017). Ilustrēts Organiskās ķīmijas vārdnīca: etilacetāts (EtOAc). Saturs iegūts no: chem.ucla.edu
- Graham Solomons T.W., Craig B. Fryhle. (2011). Organiskā ķīmija. Amīni (10. \ Tth izdevumā.). Wiley Plus.
- Morrison, R. T. un Boyd, R. N. (1990). Organiskā ķīmija (5. \ Tta izdevums). Redakcija Addison-Wesley Iberoamericana.
- Vikipēdija. (2019). Etilacetāts. Saturs iegūts no: en.wikipedia.org
- Cotton S. (s.f.). Etilacetāts. Saturs iegūts no: chm.bris.ac.uk
- PubChem. (2019). Etilacetāts. Saturs iegūts no: pubchem.ncbi.nlm.nih.gov
- Newseed Chemical. (2018). Etilacetāta pielietojums un izmantošana. Saturs iegūts no: foodsweeteners.com
- Ņūdžersijas vecāko dienestu veselības departaments. (2002). Etilacetāts. [PDF] Saturs iegūts no: nj.gov


