Atomu tilpums Kā tas mainās periodiskajā tabulā un piemēros
The atomu tilpums ir relatīvā vērtība, kas norāda attiecību starp elementa molu masu un tā blīvumu. Tātad šis tilpums ir atkarīgs no elementa blīvuma, un blīvums ir atkarīgs no fāzes un no tā, kā atomi ir izvietoti tajā..
Tātad Z elementa atomu tilpums citā fāzē atšķiras no tā, kas parādās istabas temperatūrā (šķidrums, ciets vai gāze), vai ja tas ir daļa no atsevišķiem savienojumiem. Tādējādi Z atoma tilpums savienojumā ZA atšķiras no Z Z Z savienojumā.

Kāpēc? Lai to saprastu, ir nepieciešams salīdzināt atomus ar, piemēram, marmoriem. Marmors, tāpat kā augstākā attēla zilās krāsas, ir ļoti labi definējis savu materiālo robežu, kas tiek novērota pateicoties tās izcilajai virsmai. Turpretī atomu robeža ir difūza, lai gan tos var uzskatīt par sfēriskiem attālumiem.
Tādējādi tas, kas nosaka punktu, kas pārsniedz atomu robežu, ir nulles varbūtība atrast elektronu, un šis punkts var būt tālāk vai tuvāk kodolam atkarībā no tā, cik daudz kaimiņu atomu mijiedarbojas ap atomu..
Indekss
- 1 Atomu tilpums un rādiuss
- 2 Papildu formula
- 3 Kā atomu tilpums periodiskajā tabulā mainās?
- 3.1 Pārejas metālu atomu tilpumi
- 4 Piemēri
- 4.1 1. piemērs
- 4.2. 2. piemērs
- 5 Atsauces
Atomu tilpums un rādiuss
Mijiedarbojoties ar diviem H atomiem H molekulā2, to kodolu atrašanās vietas ir definētas, kā arī attālumi starp tiem (starpkodolu attālumi). Ja abi atomi ir sfēriski, rādiuss ir attālums starp kodolu un izkliedēto robežu:
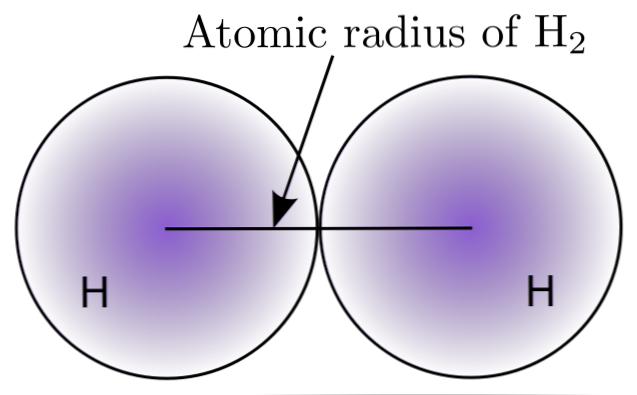
Augšējā attēlā var redzēt, kā varbūtība atrast elektronu samazinās, kad tā pārvietojas prom no kodola. Sadalot starpkodolu attālumu starp diviem, iegūst atomu rādiusu. Tālāk, pieņemot, ka atomiem ir sfēriska ģeometrija, mēs izmantojam formulu, lai aprēķinātu sfēras tilpumu:
V = (4/3) (Pi) r3
Šajā izteiksmē r ir H molekulai noteiktais atomu rādiuss2. Vērtība, ko aprēķina ar šo neprecīzo metodi, var mainīties, ja, piemēram, tā tika uzskatīta par H2 šķidrā vai metāliskā stāvoklī. Tomēr šī metode ir ļoti neprecīza, jo atomu formas ir tālu no ideālās sfēras to mijiedarbībā..
Lai noteiktu atomu tilpumus cietvielās, tiek ņemti vērā daudzi mainīgie, kas attiecas uz izkārtojumu, un tos iegūst, izmantojot rentgenstaru difrakcijas pētījumus..
Papildu formula
Molu masa izsaka vielas daudzumu, kas satur vienu molu ķīmiskā elementa atomu.
Tās vienības ir g / mol. No otras puses, blīvums ir tilpums, kas aizņem vienu gramu elementa: g / ml. Tā kā atomu tilpuma vienības ir ml / mol, jums ir jāspēlē ar mainīgajiem lielumiem, lai sasniegtu vēlamo vienību:
(g / mol) (ml / g) = ml / mol
Vai arī tas pats:
(Molārā masa) (1 / D) = V
(Molārā masa / D) = V
Tādējādi var viegli aprēķināt elementa atomu viena mola tilpumu; kamēr ar sfēriskā tilpuma formulu tiek aprēķināts atsevišķa atoma tilpums. Lai sasniegtu šo vērtību no pirmās, ir nepieciešama konversija, izmantojot Avogadro numuru (6.02 · 10).-23).
Kā atoma tilpums periodiskajā tabulā atšķiras?
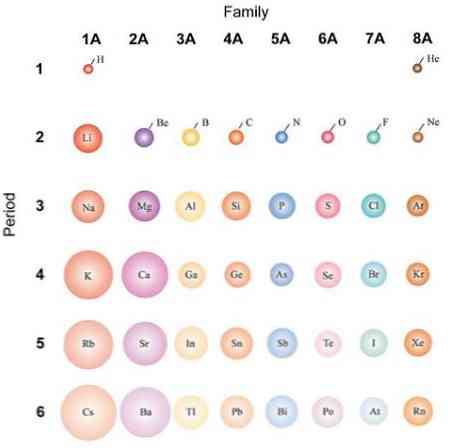
Ja atomi tiek uzskatīti par sfēriskiem, tad to variācija būs tāda pati kā atomu rādiusos. Augšējā attēlā, kas attēlo reprezentatīvos elementus, ir parādīts, ka no labās puses uz kreiso pusi atomi punduri; tā vietā no augšas uz leju tie kļūst apjomīgāki.
Tas ir tāpēc, ka tajā pašā periodā kodols ietver protonus, kad tas pārvietojas pa labi. Šie protoni rada pievilcīgu spēku uz ārējiem elektroniem, kas jūtas efektīvs kodolmateriālu lādiņš Zef, mazāk nekā faktiskā kodolmateriāla maksa Z.
Iekšējo slāņu elektroni atgrūž ārējā slāņa elektronus, samazinot kodola ietekmi uz tiem; Tas ir pazīstams kā ekrāna efekts. Tajā pašā laika posmā ekrāna efekts nespēj novērst protonu skaita pieaugumu, tāpēc elektroni iekšējā slānī neaizkavē atomu kontrakciju..
Tomēr, nolaižoties grupā, tiek aktivizēti jauni enerģijas līmeņi, kas ļauj elektroniem orbītēt tālāk no kodola. Arī palielinās elektronu skaits iekšējā slānī, kuru aizsargājošie efekti sāk samazināties, ja kodols atkal pievieno protonus.
Šo iemeslu dēļ ir redzams, ka 1.A grupai ir vislielākie atomi, atšķirībā no 8.A grupas (vai 18. grupas) mazajiem atomiem, cēlgāzēm..
Pārejas metālu atomu tilpums
Pārejas metālu atomi iekšējos orbitālos ietver elektronus d. Šis ekrāna efekta pieaugums, kā arī reālā kodolenerģijas maksa Z, tiek atcelts gandrīz vienādi, lai to atomi saglabātu līdzīgu izmēru tajā pašā periodā.
Citiem vārdiem sakot: vienā periodā pārejas metāliem piemīt līdzīgi atomu tilpumi. Tomēr šīs mazās atšķirības ir ārkārtīgi nozīmīgas, definējot metāliskos kristālus (it kā tie būtu metāla marmori)..
Piemēri
Ir pieejamas divas matemātiskas formulas, lai aprēķinātu elementa atomu tilpumu, katrs ar atbilstošiem piemēriem.
1. piemērs
Ņemot vērā ūdeņraža atomu rādiusu - 37 pm (1 pikometrs = 10. \ T-12m) - un cēzija -265 pm - aprēķina tā atomu tilpumus.
Izmantojot sfēriskā apjoma formulu, mums ir:
VH= (4/3) (3.14.) (37 pm)3= 212,07 pm3
VCs= (4/3) (3.14.) (265)3= 77912297,67 pm3
Tomēr šie tilpumi, kas izteikti pirometros, ir pārmērīgi lieli, tāpēc tos pārveido angstromu vienībās, reizinot tos ar konversijas koeficientu (1 / 100pm).3:
(212.073) (1 / 100pm)3= 2,1207 × 10-4 Å3
(77912297,67 pm)3) (1 / 100pm)3= 77,912 Å3
Līdz ar to lieluma atšķirības starp mazo H atomu un lielajiem Cs atomiem paliek skaitliski skaidrs. Jāatceras, ka šie aprēķini ir tikai aptuvenie apgalvojumi, apgalvojot, ka atoms ir pilnīgi sfērisks, kas klīst ar realitāti.
2. piemērs

Tīra zelta blīvums ir 19,32 g / ml un tā molārā masa ir 196,97 g / mol. Piemērojot formulu M / D, lai aprēķinātu viena mola zelta atomu apjomu, ir:
VAu= (196,97 g / mol) / (19,32 g / ml) = 10,19 ml / mol
Tas ir, ka 1 mols zelta atomu aizņem 10,19 ml, bet kāda tilpuma zelta atomam ir īpaša nozīme? Un kā to izteikt pm vienībās3? Šim nolūkam vienkārši izmantojiet šādus pārrēķina koeficientus:
(10,19 ml / mol) · (mol / 6.02 · 10)-23 atomi) · (1 m / 100 cm)3· (13:00 / 10-12m)3= 16,92 · 106 pm3
No otras puses, zelta atomu rādiuss ir 166 pm. Ja jūs salīdziniet abus sējumus - to, kas iegūts ar iepriekšējo metodi, un to, kas aprēķināta ar sfēriskā tilpuma formulu - jūs atradīsiet, ka tiem nav tādas pašas vērtības:
VAu= (4/3) (3,14) (166 pm)3= 19,15 · 106 pm3
Kurš no šiem diviem ir vistuvāk pieņemtajai vērtībai? Tas, kas ir vistuvāk eksperimentālajiem rezultātiem, kas iegūti ar zelta kristāliskās struktūras rentgena difrakciju.
Atsauces
- Helmenstine, Anne Marie, Ph.D. (2017. gada 9. decembris). Atomu apjoma definīcija. Saturs saņemts 2018. gada 6. jūnijā no: thinkco.com
- Mayfair, Andrew. (2018. gada 13. marts). Kā aprēķināt Atom apjomu. Science. Saturs iegūts 2018. gada 6. jūnijā no: sciencing.com
- SIA Wiki Kids (2018). Lothar Meyer atomu tilpuma līknes. Saturs saņemts 2018. gada 6. jūnijā no: wonderwhizkids.com
- Lūmena Periodiskas tendences: atomu rādiuss. Saturs iegūts 2018. gada 6. jūnijā no: courses.lumenlearning.com
- Camilo J. Derpich. Apjoms un atomu blīvums. Saturs iegūts 2018. gada 6. jūnijā no: es-puraquimica.weebly.com
- Whitten, Davis, Peck & Stanley. Ķīmija (8. izdevums). CENGAGE Learning, 222-224. Lpp.
- CK-12 fonds. (2010. gada 22. februāris). Salīdzinoši atomu izmēri. [Attēls] Saturs iegūts 2018. gada 6. jūnijā no: commons.wikimedia.org
- CK-12 fonds. (2010. gada 22. februāris). H atoma rādiuss2. [Attēls] Saturs iegūts 2018. gada 6. jūnijā no: commons.wikimedia.org


