Eksotermiskās reakcijas process, veidi un piemēri
The eksotermiska reakcija ir ķīmiskās reakcijas veids, kurā notiek enerģijas pārnešana, galvenokārt siltuma vai gaismas izdalīšanās veidā. Nosaukums nāk no Grieķijas prefiksa ekso, kas nozīmē "ārzemēs"; un termins "termiskā", kas attiecas uz siltumu vai temperatūru.
Šajā ziņā eksotermiskās reakcijas var nodot cita veida enerģiju videi, kurā tās rodas, piemēram, ar sprādzieniem un to veidu, kā nodot kinētisko un skaņas enerģiju, kad tiek paplašinātas vielas, kas atrodas gāzveida fāzē augstās temperatūrās. vardarbīgā veidā.
Tādā pašā veidā bateriju izmantošanas gadījumā tiek veikta arī eksotermiska reakcija, tikai šajā gadījumā tiek transportēta elektroenerģija..
Indekss
- 1 Process
- 2 veidi
- 2.1. Degšanas reakcijas
- 2.2 Neitralizācijas reakcijas
- 2.3. Oksidācijas reakcijas
- 2.4 Termītu reakcija
- 2.5. Reakcijas polimerizācija
- 2.6 Kodoldalīšanās reakcija
- 2.7 Citas reakcijas
- 3 Piemēri
- 4 Atsauces
Process
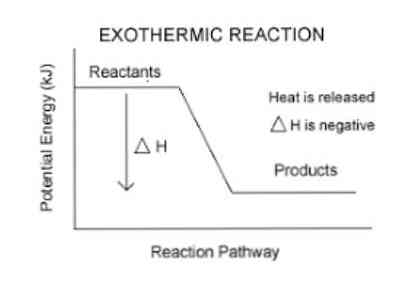
Iepriekš tika minēts, ka tad, kad notiek eksotermiska reakcija, notiek enerģijas atbrīvošanās, ko var vieglāk vizualizēt šādā vienādojumā:
Reaģenti → Produkts (-i) + enerģija
Tātad, lai noteiktu sistēmas absorbēto vai izdalīto enerģiju, izmanto termodinamisko parametru, ko sauc par entalpiju (apzīmēts ar "H"). Ja sistēmā (šajā gadījumā ķīmiskā reakcija) apkārtējā vidē ir enerģija, tad entalpijas variācija (izteikta ΔH) būs negatīva..
Pretējā gadījumā, ja šī pasākuma variācija ir pozitīva, tā atspoguļo siltuma absorbciju no apkārtnes. Turklāt sistēmas entalpijas variācijas lielums ir enerģijas daudzums, kas tiek pārnests uz vidi vai no tās..
Jo lielāks ir ΔH lielums, jo lielāka ir enerģijas izdalīšanās no sistēmas uz apkārtējo vidi.
Tas ir tāpēc, ka šajās reakcijās tīrā enerģija, kas tiek izlaista, kad tiek radītas jaunas saites, ir lielāka nekā neto enerģija, ko izmanto saikņu sadrumstalotībā.
No iepriekš minētā var secināt, ka šāda veida reakcijas ir ļoti bieži sastopamas, jo reakcijas produktiem ir enerģijas daudzums, kas tiek uzglabāts saitēs, kas ir lielākas par to, kas ir reaktīvos..
Veidi
Dažādās ķīmijas nozarēs ir gan eksotermiskas reakcijas, gan laboratorijā, gan rūpniecībā; Daži no tiem tiek veikti spontāni, bet citiem ir nepieciešami īpaši apstākļi vai kāda veida viela, piemēram, katalizators.
Svarīgākie eksotermisko reakciju veidi ir šādi:
Degšanas reakcijas
Degšanas reakcijas ir tādas, kas rodas no redoksveida veida, kas rodas, ja viena vai vairākas vielas reaģē ar skābekli, parasti, lai radītu gaismu un siltumenerģiju, tas ir, gaismu un siltumu, kad tiek veidota liesma..
Neitralizācijas reakcijas
Neitralizācijas reakcijas raksturo mijiedarbība starp skābes sugu un sārmu vielu (bāzi), lai veidotu sāli un ūdeni, kas izpaužas eksotermiskā veidā..
Oksidācijas reakcijas
Ir daudz šāda veida reakciju, kas uzrāda eksotermisku uzvedību, jo skābekļa oksidēšana izraisa lielu enerģijas daudzumu, kā tas notiek ogļūdeņražu oksidēšanā..
Termītu reakcija
Šī reakcija var radīt aptuveni 3000 ° C temperatūru, un, pateicoties alumīnija pulvera lielajai afinitātei ar lielu skaitu metāla oksīdu, to izmanto tērauda un dzelzs metināšanai..
Polimerizācijas reakcija
Šāda veida reakcija ir tāda, kas rodas, kad reaģē uz noteiktu skaitu ķīmisko vielu, ko sauc par monomēriem, kas ir vienības, kuras kombinējot tiek atkārtotas ķēdēs, veidojot makromolekulāras struktūras, ko sauc par polimēriem..
Kodoldalīšanās reakcija
Šis process attiecas uz atomu, kas uzskatāms par smagu, ti, ar masas numuru (A), lielāku par 200, sadalīšanu), lai iegūtu mazāka izmēra fragmentus vai kodolus ar vidējo masu..
Šajā reakcijā, kad ir izveidots viens vai vairāki neitroni, tiek atbrīvots liels enerģijas daudzums, jo kodolam ar lielāku svaru ir zemāka stabilitāte nekā tās produktiem..
Citas reakcijas
Ir arī citas ļoti nozīmīgas eksotermiskas reakcijas, piemēram, dažu ogļhidrātu dehidratācija, reaģējot ar sērskābi, ūdens absorbcija, kas satur nātrija hidroksīdu, kas pakļauts atklātajam gaisam, vai metālu sugu oksidēšanās daudzās korozijas reakcijās..
Piemēri
Zemāk ir daži eksotermisko reakciju piemēri, kas rada entalpijas variāciju, kam ir negatīva vērtība, jo tie atbrīvo enerģiju, kā minēts iepriekš..
Piemēram, propāna sadedzināšana ir spontāna eksotermiska reakcija:
C3H8(g) + 5O2(g) → 3CO2(g) + 4H2O (l)
Vēl viens eksotermiskas uzvedības gadījums ir parādīts neitralizācijas reakcijā starp nātrija karbonātu un sālsskābi:
NaHCO3(ac) + HCl (ac) → NaCl (ac) + H2O (l) + CO2(g)
Ir sniegts arī etanola oksidēšana ar etiķskābi, ko izmanto elpceļos, kuru pilnīga reakcija ir parādīta šādā vienādojumā:
3CH3CH2OH + 2K2Kr2O7 + 8H2SO4 → CH3COOH + 2Cr (SO4)3 + 2K2SO4 + 11H2O
Vēl viena eksotermiskās reakcijas klase ir tā sauktā termīta reakcija, kurā alumīnijs ir apvienots ar metāla oksīdu, kā norādīts tālāk:
2Al (s) + Ticība2O3(s) → Al2O3(s) + Fe (l)
Papildus iepriekš paskaidrotajiem piemēriem ir arī dažādas reakcijas, kas tiek uzskatītas par eksotermiskām, piemēram, dažu organisko atkritumu sadalīšanās kompostēšanai..
Tas arī izceļ luciferīna pigmenta oksidēšanos ar luciferāzes enzīmu iedarbību, lai iegūtu daudzu citu reakciju bioluminescenci, kas raksturīga fireflijiem, un pat elpošanu..
Atsauces
- Vikipēdija. (s.f.). Eksotermiska reakcija. Izgūti no es.wikipedia.org
- BBC (s.f.). Enerģijas izmaiņas un atgriezeniskas reakcijas. Izgūti no bbc.co.uk
- Chang, R. (2007). Ķīmija, devītais izdevums. (McGraw-Hill).
- Walker, D. (2007). Ķīmiskās reakcijas. Izgūti no books.google.co.ve
- Saunders, N. (2007). Ķīmisko reakciju izpēte. Izgūti no books.google.co.ve


