Fenantrēna ķīmiskā struktūra, īpašības un pielietojumi
The fenantrēns tā ir ogļūdeņraža (tā struktūra ir ogleklis un ūdeņradis), kuras fizikālās un ķīmiskās īpašības ir pētītas ar organisko ķīmiju. Tas pieder tā saukto aromātisko savienojumu grupai, kuras pamata struktūrvienība ir benzols.
Aromātiskie savienojumi ietver arī kausētos policikliskos savienojumus, ko veido vairāki aromātiskie gredzeni, kuriem ir oglekļa-oglekļa (C-C) saite. Fenantrēns ir viens no tiem, tajā ir trīs savienoti gredzeni. Tiek uzskatīts par antracēna izomēru - savienojumu, kura trīs gredzeni ir sapludināti lineāri.
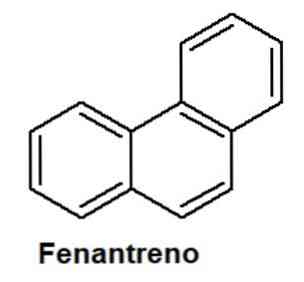
Tas tika izdalīts no antracēna eļļas no akmeņogļu darvas. To iegūst, destilējot koksni, transportlīdzekļu emisijas, naftas noplūdes un citus avotus..
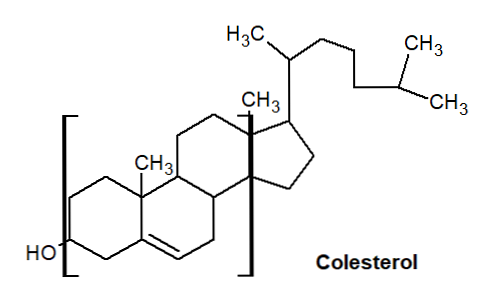
Tā atrodas vidē, izmantojot cigarešu dūmus, un steroīdu molekulās tā veido ķīmiskās struktūras aromātisko pamatu, kā parādīts holesterīna molekulā..
Indekss
- 1 Ķīmiskā struktūra
- 2 Fizikālās un ķīmiskās īpašības
- 3 Lietojumi
- 3.1 Farmakoloģija
- 4 Ietekme uz veselību
- 5 Atsauces
Ķīmiskā struktūra
Fenantrēnam ir ķīmiska struktūra, ko veido trīs benzola gredzeni, kas savienoti kopā ar oglekļa-oglekļa saiti.
Tas ir uzskatāms par aromātisku struktūru, jo tas atbilst Hückle likumam par aromātiku, kurā teikts: "Savienojums ir aromātisks, ja tam ir 4n + 2 pi (π) delokalizēti un konjugēti (pārmaiņus) elektroni, ar sigma elektroniem (σ) no vienkāršas saites.
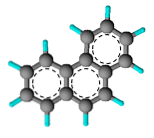
Piemērojot Hückel likumu fenantrēna struktūrai un ņemot vērā to, ka n atbilst struktūrā esošo benzola gredzenu skaitam, izrādās, ka 4n + 2 = 4 (3) +2 = 16 elektroni π. Tie tiek uzskatīti par divkāršām saitēm molekulā.
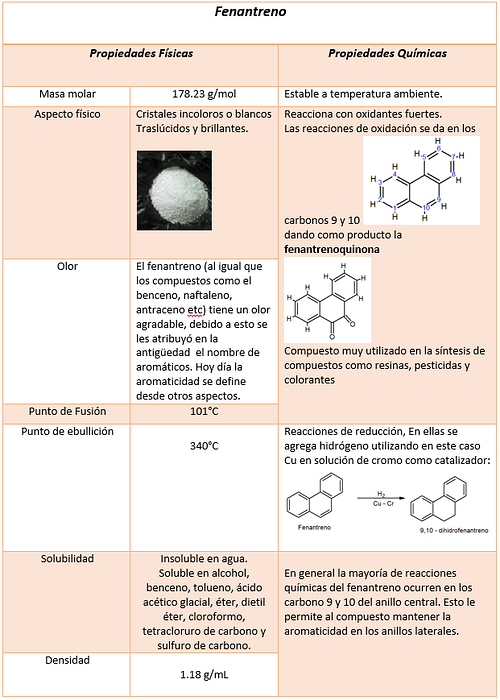
Fizikālās un ķīmiskās īpašības
-Blīvums 1180 kg / m3; 1,18 g / cm3
-Kušanas punkts 489,15 K (216 ° C)
-Viršanas punkts 613,15 K (340 ° C)
Savienojuma īpašības ir īpašības vai īpašības, kas ļauj to atšķirt no citiem. Īpašības, ko mēra savienojumam, ir fizikālās īpašības un ķīmiskās īpašības.
Kaut arī fenantrēns ir antracēna izomēra forma, tā īpašības ir ļoti atšķirīgas, dodot fenantrēna lielāku ķīmisko stabilitāti viena no tā aromātisko gredzenu leņķa pozīcijas dēļ..
Lietojumi
Farmakoloģija
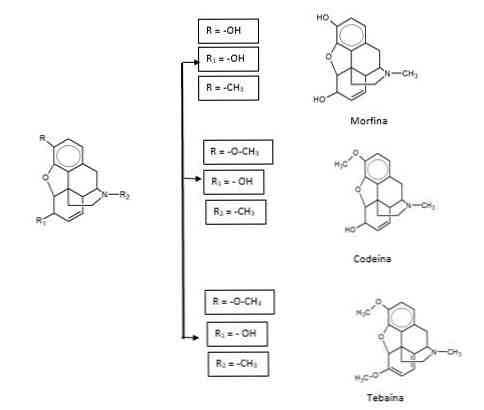
Opioīdu zāles var būt dabiskas izcelsmes vai fenantrēna atvasinājumi. To vidū ir morfīns, kodeīns un tebaīns.
Fenantrēna reprezentatīvākie lietojumi tiek iegūti oksidētā veidā; tas ir, fenantrenekvinons. Tādā veidā to var izmantot kā krāsvielas, zāles, sveķus, fungicīdus un dažu procesu polimerizācijas inhibēšanu. 9,10-bifenildikarboksilskābi izmanto poliestera un alkīda sveķu ražošanai.
Ietekme uz veselību
Ne tikai fenantrēns, bet visi policikliskie aromātiskie ogļūdeņraži, ko parasti sauc par PAH, ir toksiski un kaitīgi veselībai. Tie ir atrodami ūdenī, uz zemes un gaisā, kas radušies sadegšanas, naftas noplūdes vai kā reakcijas rezultātā rūpniecībā..
Toksiskums palielinās, jo to ķēdes ar kausētajiem benzola gredzeniem kļūst arvien lielākas, lai gan tas nenozīmē, ka īstermiņa ķēdes PAH nav..
No benzola, kas ir šo savienojumu galvenā struktūrvienība, jau ir zināms tās augstais toksiskums un mutagēna iedarbība dzīvajās būtnēs..
Naftalīnu, ko sauc par kodēm, izmanto kā kaitīgo organismu, kas uzbrūk apģērba audumiem, kontroli. Antracēns ir mikrobicīds, ko lieto tabletes, lai novērstu baktēriju izraisītās smakas.
Fenantrēna gadījumā tas uzkrājas dzīvo būtņu taukaudos, radot toksicitāti, ja indivīds ilgstoši tiek pakļauts piesārņotājam..
Papildus šīm sekām var minēt šādus nosaukumus:
- Tas ir degviela.
- Pēc ilgstošas fenantrēna iedarbības indivīds var klepus, elpošanas traucējumi, bronhīts, elpceļu kairinājums un ādas kairinājums..
- Sildot līdz sadalīšanās procesam, var izraisīt ādas un elpceļu kairinājumu, ko izraisa blīvs un nosmakojošs dūms.
- Var reaģēt ar stipriem oksidētājiem.
- Ugunsgrēka gadījumā, kad notiek šis savienojums, to var kontrolēt ar sausu oglekļa dioksīdu, halona ugunsdzēšamo aparātu vai ar ūdens strūklu.
- Tas jāuzglabā vēsās vietās, hermētiskā traukā un prom no oksidējošām vielām.
- Būtu jālieto individuālie aizsardzības līdzekļi (MMP), pārklāti apavi, garās piedurknes priekšauts un cimdi.
- Saskaņā ar Darba drošības un veselības aizsardzības valsts institūtu, lai apstrādātu šo savienojumu, jāizmanto pus-sejas maska, kas aprīkota ar pret miglas filtriem, un vēl viens īpašs ķīmisko tvaiku filtrs..
- Acu un / vai ādas kairinājuma gadījumā ieteicams mazgāt ar lielu daudzumu ūdens, noņemt piesārņotos apģērbus vai piederumus un ļoti nopietnos gadījumos nodot pacientam medicīnisko palīdzību..
Atsauces
- ScienceDirect, (2018), fenantēns, atgūts, arzo 26 no 2018. gada, sciencedirect.com
- Mastandrea, C., Chichizola, C., Ludueña, B., Sánchez, H., Alvarez, H., Gutiérrez, A., (2005). Policikliskie aromātiskie ogļūdeņraži. Veselības riski un bioloģiskie marķieri, Latīņamerikas klīniskās bioķīmijas likums, 39,1, scielo.org.ar
- Beyer, H., Wolfgang, W., (1987), Organiskās ķīmijas rokasgrāmata (E-Book), books.google.com.co
- Cheimicalbook, (s.f), fenantrēns, fenantēns Ķīmiskās īpašības un informācija par drošību, atjaunota, 2018. gada 26. marts, chemicalbook.com
- Fernández, P L., (1996), sāpju farmakoloģiskā ārstēšana, opiātu zāles, kas iegūtas no fenantrēna, UCM, Madride, [PDF], ucm.es, revistas.ucm.es
- Cameo Chemicals, (s.f), fenantēns, datu lapa un drošība, izgūta, 2018. gada 27. marts, cameochemicals.noaa.gov
- Morrison, R., Boyds, R., (1998), Organic Chemistry (5. izdevums), Meksika, Amerikāņu izglītības fonds, S.A de C.V
- Pine, S., Hammond, G., Cram, D., Hendrickson, J., (1982). Química Orgánica, (otrais izdevums), Meksika, McGraw-Hill de México, S.A de C.V
- Chemsketch. Programmatūra, ko izmanto dažādu ķīmisko savienojumu formulu un molekulāro struktūru rakstīšanai. Darbvirsmas lietojumprogramma.


